
巨噬细胞极化作为免疫研究的核心方向,其功能亚型(M1促炎、M2抗炎等)的精准检测,是解析免疫调控机制、开展药物筛选的基础。在上一篇文章《巨噬细胞功能与检测技术丨巨噬细胞极化:机制、方案与实验要点》中,我们已经梳理了极化的分类、实验方案及核心质控要点,为科研人员提供了标准化的实验框架。
但在实际科研中,一个令人困扰的现象屡见不鲜:即便采用相同的细胞系、一致浓度的刺激剂(如LPS+IFNγ诱导M1、IL-4诱导M2a),并检测公认的极化标志物,不同实验室或同一实验室的不同批次实验,结果却常常存在差异——有的能清晰捕捉到标志物高表达,有的却出现“假阴性”,让科研人员陷入困惑。是什么导致了这种差异?除了细胞状态、试剂纯度等常见因素,极化时间或许是被忽视的潜在原因之一。
2022年的一项研究《Effect of stimulation time on the expression of human macrophage polarization markers》,以人单核细胞来源巨噬细胞(MDMs)为模型,通过系统的时间序列分析证实:时间会显著影响极化标志物的表达强度与峰值特征,这一发现为解读实验差异提供了全新视角,也为科研人员在实验陷入瓶颈时,提供了一个值得排查的新方向。
为了厘清时间与极化检测的关联,研究团队以更贴近人体生理状态的人类单核细胞来源的巨噬细胞(MDMs) 为模型(避免了THP-1等细胞系与原代细胞的差异干扰),设计了系统的对照实验,专门探索时间对极化标志物的影响:

极化亚型:覆盖M1(LPS+IFNγ诱导)、M2a(IL-4诱导)、M2c(IL-10诱导)三大核心科研常用亚型;
刺激时间:设置4 h、8 h、12 h、24 h、48 h、72 h六个梯度时间点,全面覆盖短期至长期极化过程;
检测维度:同步分析mRNA(基因转录)、表面蛋白(流式细胞术)、分泌型细胞因子(ELISA)三类核心标志物,多维度捕捉时间的潜在作用;
对照设置:以未极化的M0巨噬细胞为空白对照,确保结果的特异性与可靠性。
这项研究的核心价值,并非关注“是否极化”,而是系统呈现了不同亚型、不同检测维度中,标志物随时间变化的动态轨迹,为理解“时间为什么重要”提供了直接证据。
研究结果显示,无论是同一极化亚型的不同标志物,还是不同极化亚型的同类标志物,其表达都呈现出鲜明的“时间节律”,这种节律可能正是导致实验结果差异的重要原因:

M1作为经典促炎亚型,其标志物并非“同步激活”,而是呈现明显的时间分层特征:
mRNA层面(基因转录):CXCL9、CXCL10(趋化因子)、TNF(肿瘤坏死因子)属于“早期响应标志物”,刺激后4 h即达到表达峰值,之后逐渐下降;IL-1β(白介素-1β)在4h升高后保持稳定表达;IDO1(免疫调节相关酶)则为“晚期持续升高型”,随时间推移不断上调,48-72 h达到最高值;IL-12的表达更具特殊性,呈现“双峰模式”——4h短暂升高后下降,48 h再次显著上调。(图1A-F)
表面蛋白层面(流式检测):CD86(共刺激分子)和HLA-DR(抗原呈递分子)在12 h达到表达高峰,之后因IL-10的负反馈调节逐渐下降;CD64(Fc受体)则从8 h开始持续升高,24-72 h始终维持高表达,表现出“长效稳定”的特征。(图2A-C)
细胞因子层面(ELISA检测):TNF在4-12 h分泌最为旺盛;IL-12p70从8 h开始稳定分泌,持续至72 h;IL-1β则集中在8-24 h释放,超出这个时间窗口后,检测信号会明显减弱。(图3A-C)
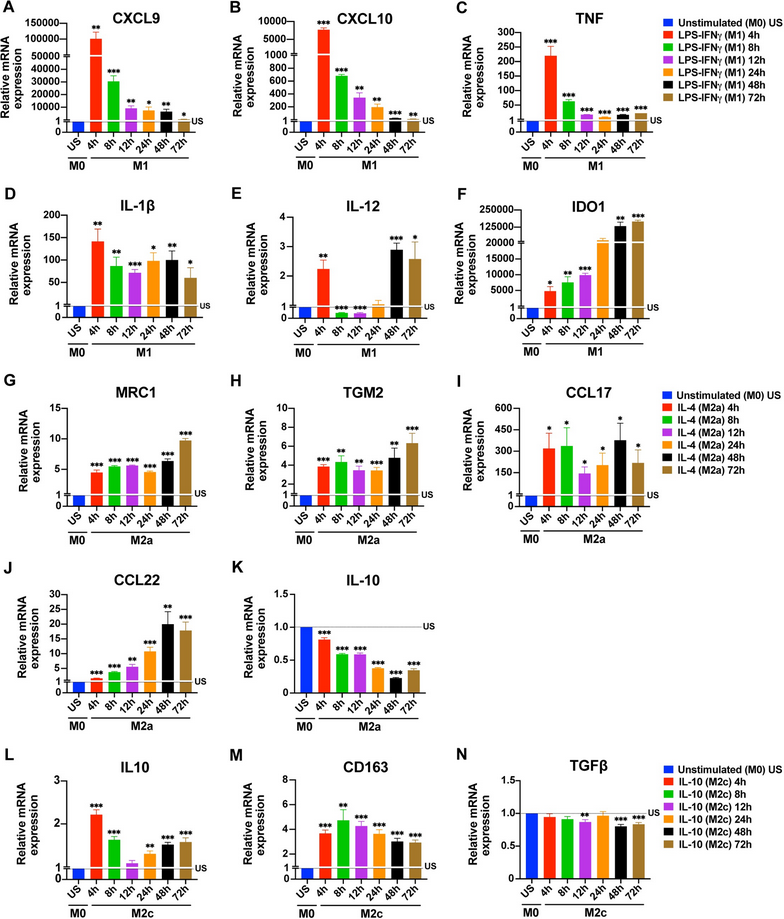
图1. Time depended changes in the expression of macrophage polarization markers at mRNA level

M2a主打组织修复、伤口愈合相关功能,其标志物表达整体偏“慢热”,与M1形成鲜明对比:
mRNA层面:CD206(甘露糖受体,MRC1)、TGM2(转谷氨酰胺酶2)从4 h开始启动表达,但直到72 h才达到峰值;CCL17(趋化因子)全程维持高表达,CCL22则从4 h逐渐升高,48 h达峰;而IL-10的mRNA水平反而随时间下降,呈现“转录与翻译不同步”的特点。(图1G-K)
表面蛋白层面:CD200R(抑制性受体)和CD206是M2a的特异性标志物,二者从8 h开始缓慢升高,48-72 h达到表达峰值,且此时标志物的特异性最强,不易与其他亚型交叉反应。(图2D-E)
细胞因子层面:IL-10的蛋白分泌在48 h后才显著检测到,印证了“转录早、翻译晚”的特点,这也意味着早期检测M2a的IL-10,很可能因未到分泌峰值而出现假阴性。(图3D)
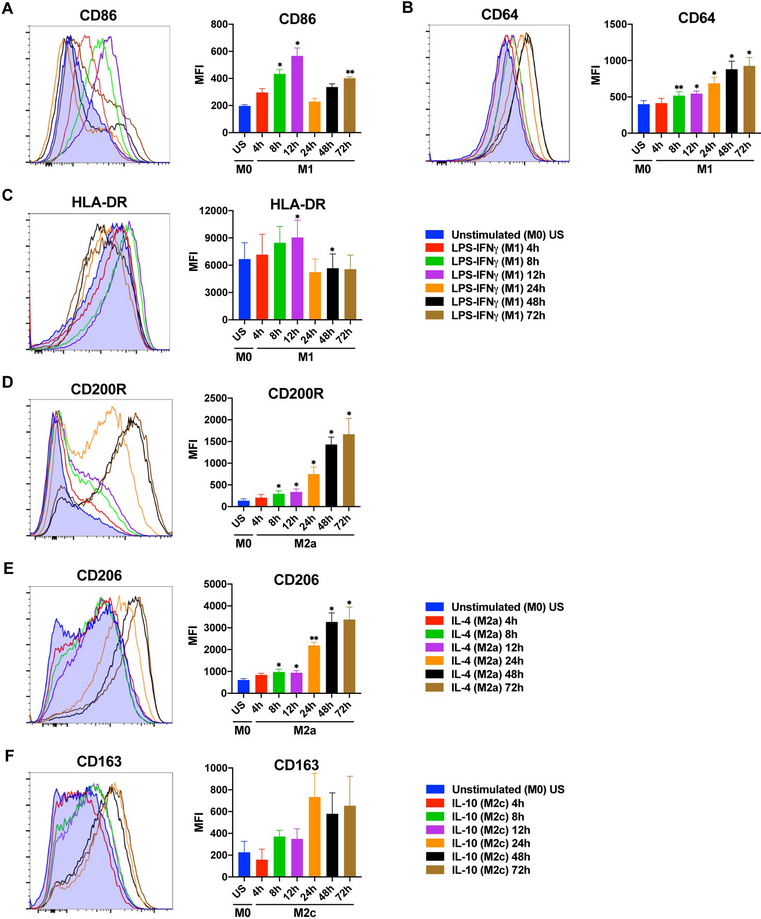
图2. Time depended changes in the expression of macrophage polarization markers at protein level

M2c由IL-10诱导,核心功能与抗炎、免疫耐受相关,其时间节律更具独特性:
mRNA层面:IL-10的基因表达在4 h就达到峰值,之后快速下降;CD163(清道夫受体)从4 h开始持续高表达,72 h仍维持稳定水平。(图1L-N)
表面蛋白层面:CD163的蛋白表达滞后于转录,24 h才开始明显升高,24-72 h是其表达的主要窗口(需注意个体差异可能对表达强度产生影响)。(图2F)
细胞因子层面:TGFβ(转化生长因子β)的mRNA全程未检测到明显信号,但蛋白分泌在72 h显著升高,说明这类细胞因子的合成与积累需要更长时间,短期检测难以捕捉到有效信号。(图3E)
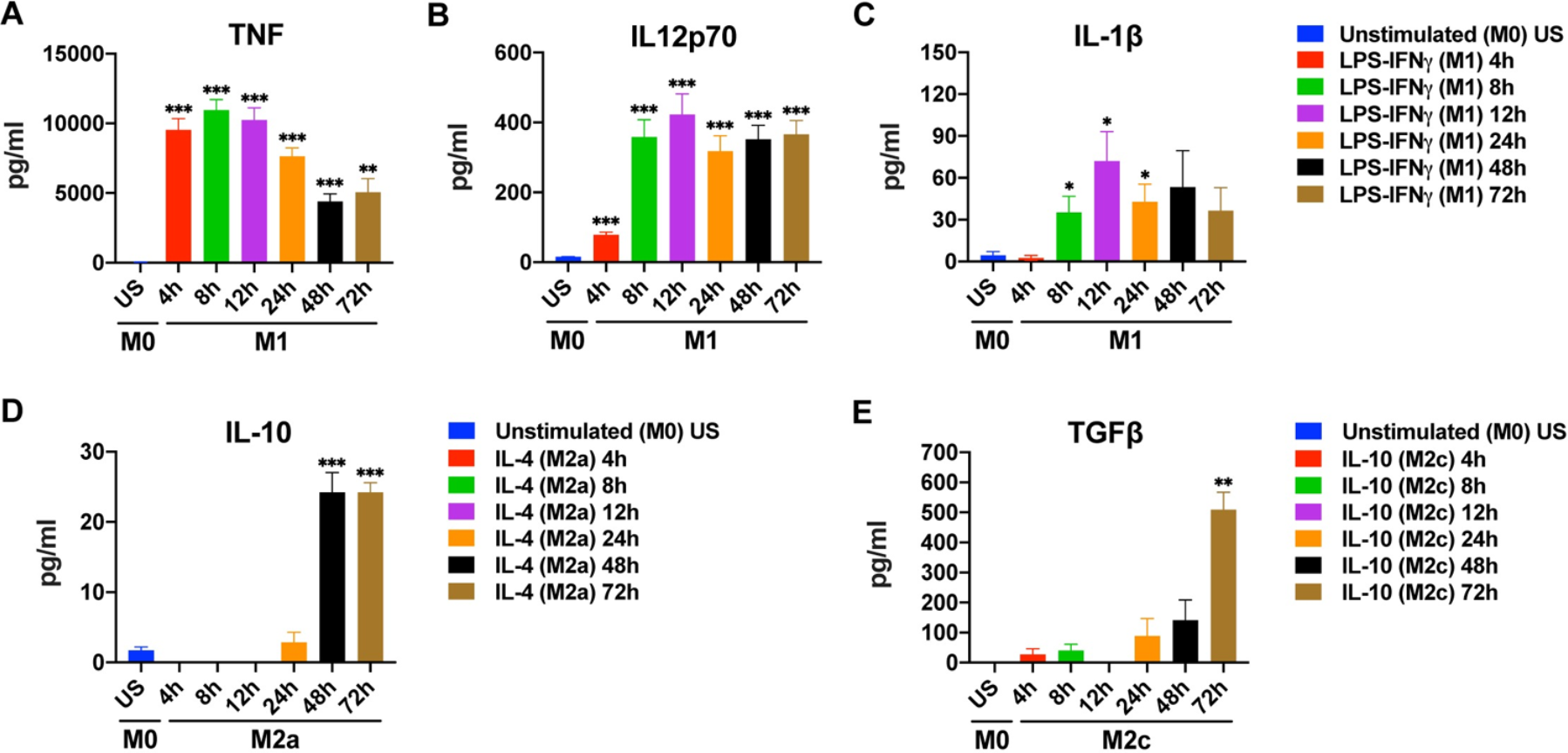
图3. Time depended changes in cytokine production by M1, M2a, and M2c macrophages
4. 细胞类型与物种的额外干扰

研究还进一步证实,时间的影响并非统一适用,还会受到细胞类型与物种的调控:人类原代巨噬细胞(MDMs)的时间节律,与THP-1等常用细胞系存在明显差异——比如THP-1对LPS的反应更弱,IL-10的表达模式与原代巨噬细胞相反。这也意味着,基于某一种细胞系得出的“时间规律”,无法直接推广到其他细胞类型或物种的研究中。
综合实验结果可以发现,巨噬细胞极化相关标志物的表达并不存在统一且稳定的时间模式。即便在相同的极化刺激条件下,不同分子在转录水平、表面表达及分泌层面的变化趋势也并不完全一致,其峰值出现的时间窗口存在明显差异。这一现象提示,在巨噬细胞极化研究中,不同研究之间关于某些标志物“是否上调”或“上调程度”的分歧,可能并非仅源于实验体系或检测方法的不同,而与检测时间点的选择密切相关。基于单一时间点获得的结果,往往难以全面反映极化过程的动态特征,也为结果解读带来一定不确定性。
三、研究启示:为科研提供新的思考维度
这项关于“时间潜在影响”的研究,并未给出统一的“最佳检测时间”标准,也无法直接用于指导实验操作,但它为巨噬细胞极化研究提供了重要的思路启发,尤其当实验陷入瓶颈时,可作为一个值得探索的方向:
巨噬细胞极化并非一个“静态终点”,而是一个受时间调控的“动态过程”。时间作为一个潜在变量,其对极化标志物表达的影响,为我们解读实验差异、排查实验瓶颈提供了全新的思路。
目前,关于时间对巨噬细胞极化的影响尚未形成统一结论,相关研究仍在探索中,但这并不影响其作为一个重要参考方向的价值。对于科研人员而言,了解这一潜在影响,能帮助我们在实验中更全面地考量变量,更理性地解读结果,甚至为机制研究找到新的切入点。未来,随着更多相关研究的开展,我们或许能逐步揭开时间调控极化的深层机制,为巨噬细胞研究提供更精准的支撑。
abinScience 巨噬细胞极化实验相关产品
1. Recombinant Proteins

(M-CSF)(GM-CSF)(TNF‐α)(IL-4)(IL-6)(IL‐10)(IL-13)
2. Flow Cytometry Antibodies

(CD11b)(CD11c)(CD14)(CD15)(CD16)(CD80)(CD86)(CD163)(CD204)(CD206)(CD209)(CD274)(F4/80)(HLA-DR)(Ly6G)(MHC-Ⅱ)(IFN-γ)(IL-1)(IL-6)(IL-12)(TNF-α)(TGF-β)(Arg-1)(iNOS)
3. Other Related Antibodies
| 标志物 | 反应性 | 名称 | 应用 | 货号 |
| iNOS | Human | Anti-NOS2 Polyclonal Antibody | ELISA, IHC, WB | HW388014 |
| Arg-1 | Human, Mouse, Rat | Anti-ARG1/Arginase-1 Polyclonal Antibody | ELISA, IHC, WB | HY339024 |
| Human, Mouse, Rat, Pig, etc | Anti-ARG1 Polyclonal Antibody | ELISA, IHC, WB | HY339014 | |
| CD11b | Human | Anti-CD11b/ITGAM Polyclonal Antibody | ELISA, IHC, WB | HY474014 |
| Mouse | Anti-Mouse CD11b/ITGAM Polyclonal Antibody | ELISA, IHC, WB | MY474014 | |
| CD86 | Human | Anti-CD86 Polyclonal Antibody | ELISA, IHC, WB | HW776014 |
| Mouse | Anti-Mouse CD86/B7-2 Polyclonal Antibody | ELISA, IHC, WB | MW776014 | |
| CD206 | Human, Mouse, Rat | Anti-CD206/MRC1 Polyclonal Antibody | ELISA, IHC, WB | HB976014 |
| IL-1 | Human, Cercocebus atys, Macaca fascicularis, etc | Anti-IL1B/IL1F2 Polyclonal Antibody | ELISA, IHC, WB | HF943014 |
| IL-6 | Human | Anti-Human IL6 Antibody | ELISA, FCM, WB, IHC, IF | HY328033 |
| Mouse | Anti-Mouse IL6 Monoclonal Antibody | ELISA, IHC, WB | MY328085 | |
| IL-10 | Human | Anti-Human IL10 Antibody | ELISA, WB, IHC, FCM | HB997023 |
| TNF-α | Human, Dog, Cat, Pig, etc | Anti-TNFa/TNF-alpha Polyclonal Antibody | ELISA, IHC, WB | HF879014 |
| Mouse, Rat, Peromyscus leucopus | Anti-TNFa/TNF-alpha Polyclonal Antibody | ELISA, IHC, WB | MF879014 | |
| Danio rerio | Anti-Zebrafish TNFa Polyclonal Antibody | ELISA, IHC, WB | ZA439014 | |
| TGF‐β | Human, Mouse, Dog, Rat, etc | Anti-TGFB1/TGF-beta-1 Polyclonal Antibody | ELISA, IHC, WB | HF977014 |
| Mouse | Anti-Mouse TGFB1/TGF-beta-1 Polyclonal Antibody | ELISA, IHC, WB | MF977014 |
abinScience提供一系列巨噬细胞极化相关的抗体和重组蛋白,广泛应用于ELISA、Western Blot、免疫组化、FCM等实验,帮助科研人员深入研究巨噬细胞的极化。更多巨噬细胞相关产品请访问abinScience官网:www.abinscience.cn。
发邮件给我们:support@abinscience.com
参考文献
Unuvar Purcu D, Korkmaz A, Gunalp S, Helvaci DG, Erdal Y, Dogan Y, Suner A, Wingender G, Sag D. Effect of stimulation time on the expression of human macrophage polarization markers. PLoS One. 2022 Mar 14;17(3):e0265196. doi: 10.1371/journal.pone.0265196. PMID: 35286356; PMCID: PMC8920204.
返回顶部