
做流式细胞实验的人,几乎都听过“抗体滴定”这个词。
有人把它当成流式实验里的“基本功”,觉得每支抗体都应该先滴定;也有人觉得它太耗时、太麻烦,甚至认为“说明书上不是都写了推荐用量吗,照着用不就行了?”
还有不少刚接触流式的新手,虽然知道“最好做滴定”,但对它到底是什么、为什么要做、真正的意义是什么,其实并没有形成清晰的认识。
事实上,流式抗体滴定并不神秘。它既不是高阶技巧,也不是可有可无的形式主义,而是一个帮助实验获得更清晰结果、更稳定数据、更合理控制成本的基础步骤。
简单来说,流式抗体滴定,就是为你的流式抗体,找到适配实验体系的最佳工作浓度。
流式实验的核心,是让带荧光标记的抗体去识别细胞上的目标抗原,再通过荧光信号来区分阳性细胞和阴性细胞。而抗体的用量,直接影响这种区分效果:
? 浓度过低:抗体数量不足以覆盖细胞上的抗原位点,阳性细胞的荧光信号会偏弱,甚至无法检测出低表达的抗原;
? 浓度过高:多余的抗体会出现非特异性结合,不仅会导致背景荧光升高,还会缩小阴阳群体的信号差距,让细胞分群模糊。
滴定的本质并不是“把信号做得越强越好”,而是通过浓度梯度测试,在抗体的特异性结合与非特异性结合之间,找到一个合理的平衡点:既能让抗体充分结合目标抗原,保证细胞分群清晰,又能抑制非特异性染色,让背景干净无干扰。
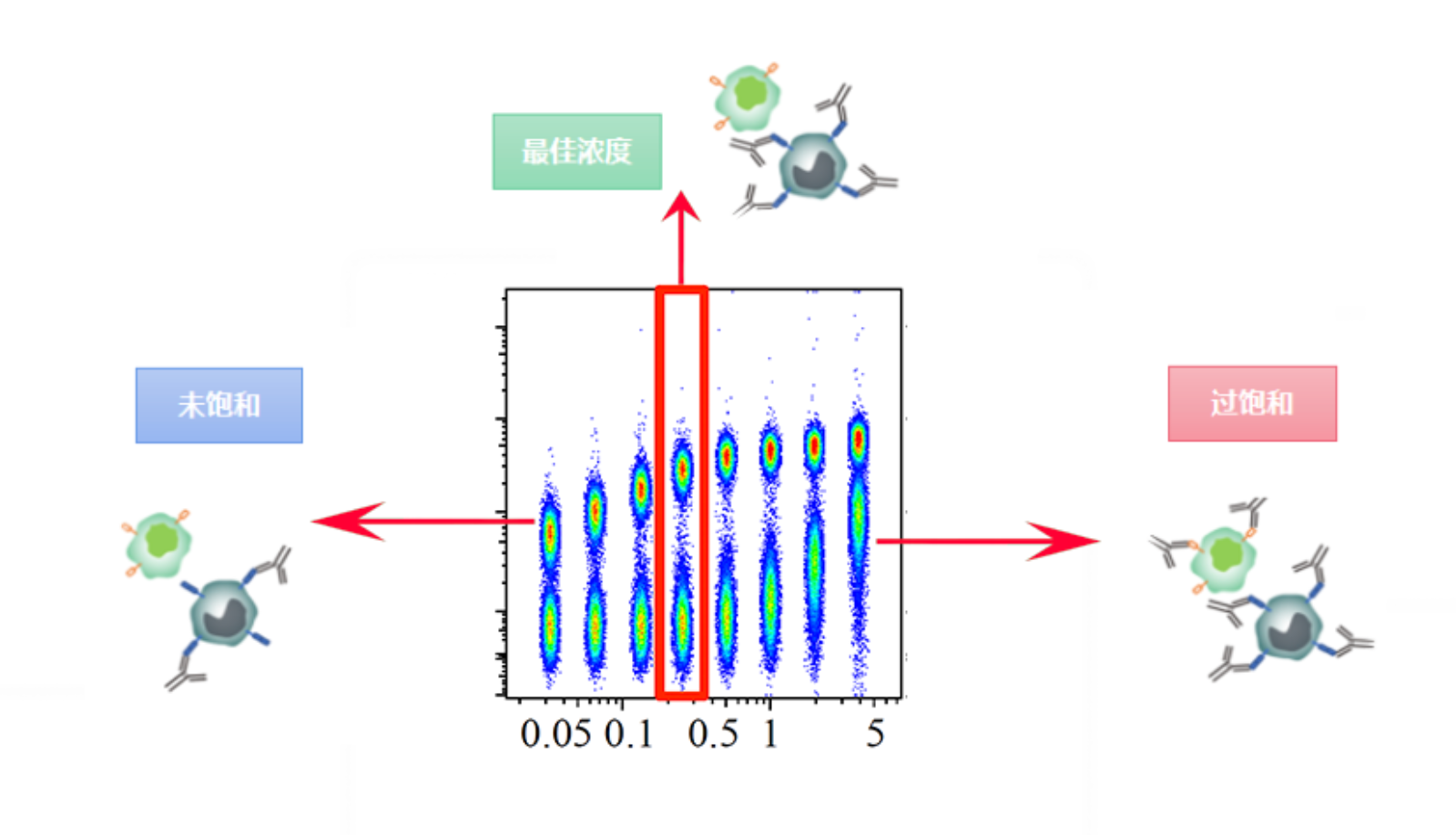
图1. 流式抗体滴定原理
? 样本:每个浓度梯度至少准备5×10?个细胞,样本类型、处理方式需要与正式实验一致;
? 梯度设置:以说明书推荐浓度为起始值,设置5-6个连续稀释梯度,覆盖不足、饱和、过量三个区间;
? 前置细节:抗体使用前可以16000-18000 g 4℃离心5 min,取上清去除聚合物;高表达Fc受体的样本提前做Fc阻断;活性低的样本先做死活染色,排除死细胞干扰。
? 固定染色体系体积、细胞数量,每管加入对应浓度的抗体,严格按照正式实验的流程操作;
? 设置空白对照、单染对照,上机前用对照设置好仪器电压等参数后,所有滴定样本全程使用同一条件采集数据,不更改任何仪器参数。
? 选择染色指数SI计算分群效果,公式:SI=(阳性群体MFI-阴性群体MFI)/(2×阴性群体荧光标准差),这个指标比单纯的信噪比更能客观反映分群效果;
? 最佳浓度选择:阴性群体背景无明显升高的前提下,SI进入平台期的最低浓度。不用盲目追求SI的最大值,多色实验中,干净的背景比峰值信号更重要。
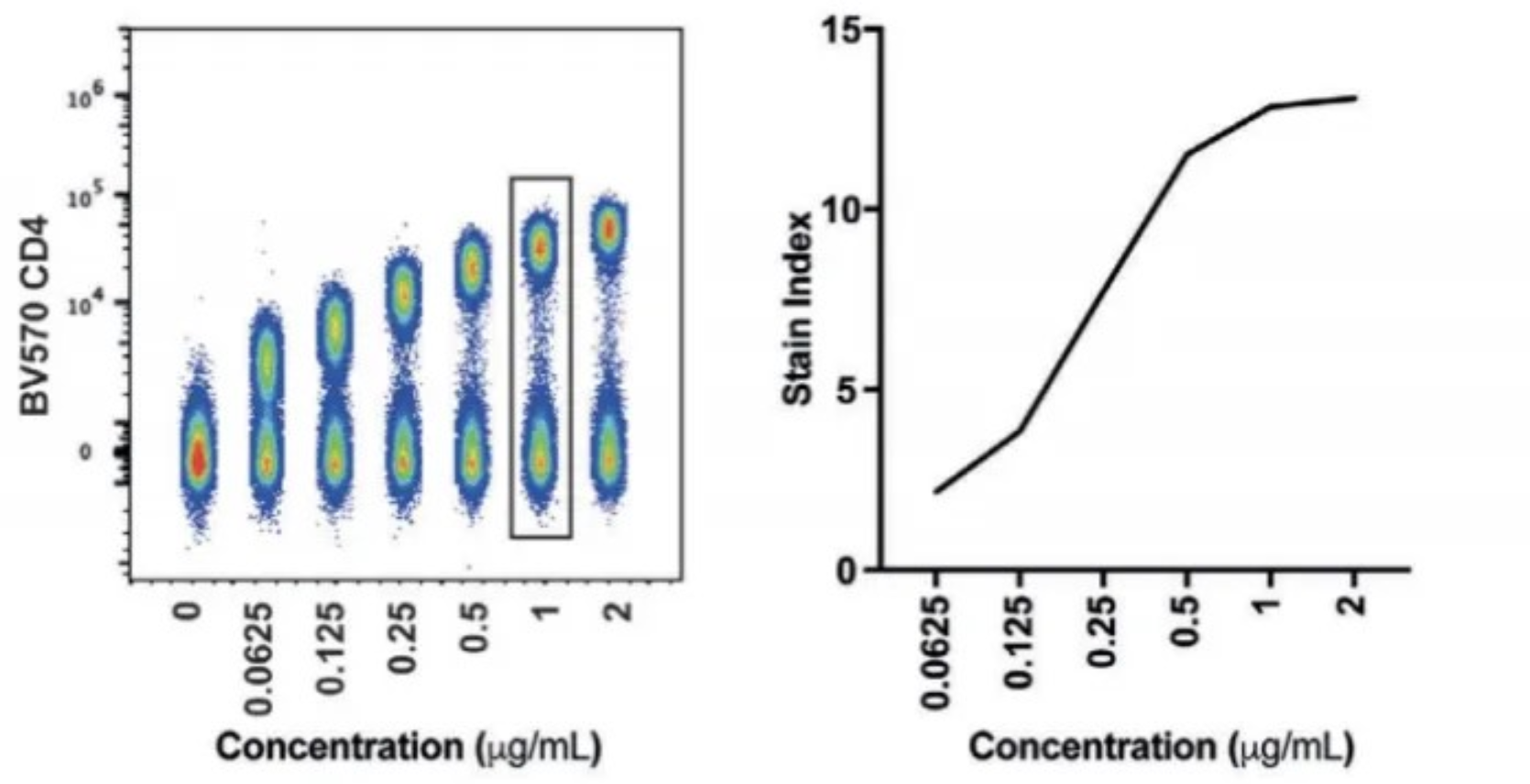
图2:BV750-CD4滴定结果
① 实验体系高度统一:滴定所用的样本类型、处理方式、细胞状态、孵育条件等,必须与正式实验完全一致,否则测试结果毫无参考价值。
② 聚焦抗体终浓度:记录滴定结果时,核心应关注终浓度而非稀释倍数,后续调整染色体系体积时,只需按终浓度同步调整抗体用量即可。
③ 固定仪器检测参数:通过对照样本调好电压等仪器参数后,所有滴定样本均在同一参数条件下完成检测,保证信号分析的客观性。
经滴定优化的浓度,能 拉开阴阳细胞群之间的信号差距,哪怕是低表达抗原的弱阳性细胞群,也能实现精准区分与计数,不会漏掉关键实验数据,这一点在高参数多色流式实验中尤为明显。
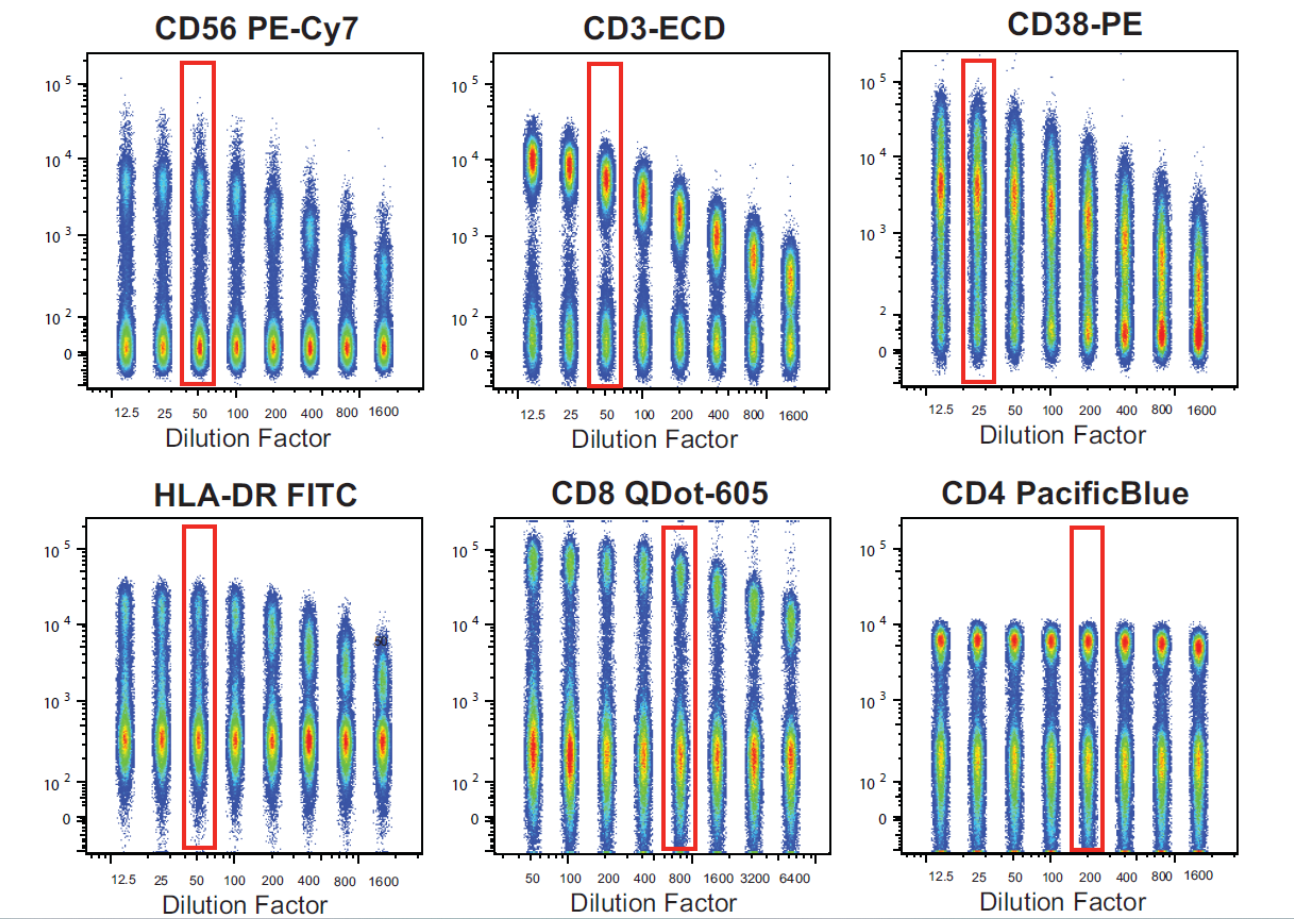
图3:不同流式抗体滴定结果展示
抗体过量带来的非特异性染色,不仅会抬高背景,还会增加荧光信号溢漏,干扰其他检测通道的结果。滴定优化后的浓度,能减少这种干扰,让整个多色检测体系更稳定。
很多人会默认抗体多加一点,信号就会更好,实际并不是这样的。滴定能帮我们找到够用且好用的最低有效浓度,在不影响实验效果的前提下,大幅延长抗体使用周期,降低长期实验的耗材成本。
科研实验最核心的要求是可重复性。固定经滴定验证的最佳浓度,能减小不同实验批次、不同操作人员带来的结果误差,让实验数据更稳定、更可靠,也更具说服力。
这是最常见的误解之一。前面已经提到,说明书上的推荐浓度通常来自标准化测试体系,而真实实验中的样本类型、处理方式、染色流程、细胞数、仪器状态都可能不同。这些变量都会影响抗体的最终表现。所以,推荐浓度是起点,不是终点。最佳浓度需要结合实际实验体系去滴定摸索。
很多人会误以为滴定要选信号峰值对应的浓度。但实际上,信号最强的点,往往是抗体过量的浓度——此时阳性信号虽强,但阴性背景也会大幅升高,阴阳群体的分群效果反而会下降。滴定真正要找的,是阴性背景无明显升高的前提下,阴阳分群效果最佳的最低浓度,而不是信号绝对值最大的点。
这是新手最常犯的错误。比如在200 μL体系中,1:200的稀释比效果很好,换到1 mL体系后仍按1:200加抗体,抗体终浓度直接翻了5倍,必然会导致抗体过量、背景飙升。
滴定的核心是抗体终浓度,而非稀释倍数。无论反应体系如何调整,只要保持终浓度不变,就能获得稳定的染色效果。
虽然SI是衡量分群的重要指标,但如果SI最高的点同时也伴随背景显著上升,在多色实验中会造成严重的通道干扰。明智的选择通常是SI曲线进入平台期后的第一个低浓度点,而非盲目追求SI数值的绝对最大。
很多人觉得,同一个货号的抗体,第一次滴定好了,后续换批次可以直接沿用结果。但事实上,即便生产工艺完全一致,不同批次的抗体在蛋白浓度、荧光偶联效率上仍会存在差异,这些差异在低表达抗原检测、多色实验中会被明显放大。因此,更换抗体批次、实验体系、样本类型后,都需要重新滴定,才能保证实验结果的稳定可靠。
总而言之,流式抗体滴定是基于自身实验体系的特性,在抗体特异性结合与非特异性结合之间找到最优平衡点,精准锁定适配实验体系的最佳工作浓度。规范的滴定既可优化流式染色分群效果、压低背景干扰、控制实验耗材成本,更能从根本上保障实验数据的稳定性与可重复性。
abinScience创立于法国,专注于高质量生命科学试剂的开发与生产,致力于为科研工作者提供高性能、高可靠性的流式抗体。针对T细胞亚群、免疫检查点、记忆/耗竭标志物等研究,我们可提供:
1. 经过严格验证的CD3、CD4、CD8等流式抗体,确保高灵敏度与低背景;
2. 覆盖Human、Mouse、Rat、Dog、Hamster等多物种的免疫学研究工具;
3. 专业的技术支持与Panel设计咨询,助您精准解析复杂免疫细胞群体。
返回顶部