
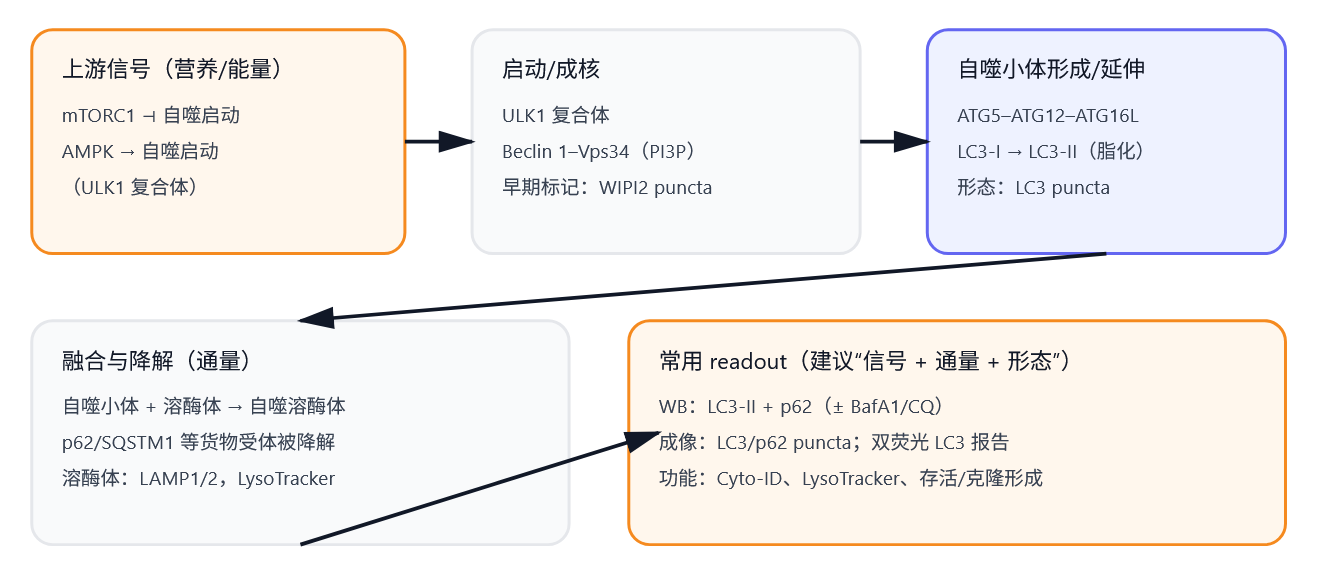
在你已经写过的 PI3K/AKT–mTOR、AMP-activated protein kinase(AMPK)等代谢与生长因子通路基础上, 宏自噬(macroautophagy,本文简称“自噬”)更像是细胞在能量与损伤压力下的“回收系统”: 通过 ULK1–Beclin 1–ATG 蛋白模块,形成双膜自噬小体,包裹受损蛋白、线粒体或其他细胞器,并与溶酶体融合完成降解。
上游抑制常来自 mechanistic target of rapamycin complex 1(mTORC1),上游激活常来自 AMPK 等能量感应轴; 但本篇不再详细展开上游信号,而是聚焦:自噬本身要测哪些指标?各自代表什么?在什么实验平台上最好用?
| 指标 | 常用位点 / 读出 | 代表意义 | 推荐样本 / 方法 | 使用提示 |
| ULK1 激活状态 | p-ULK1(Ser555 等 AMPK 位点↑;Ser757 等 mTORC1 位点↓) | 自噬起始复合体是否被“解锁”并启动 | Western blot(蛋白质印迹) | 更偏机制 readout:用于解释“上游开关是否打开”。位点体系常用框架来自 ULK1 被 AMPK 与 mTOR 直接磷酸化的研究。[3] |
| Beclin 1 / Vps34 复合体 | Beclin 1 总蛋白;与 Vps34、ATG14L 的相互作用(免疫沉淀) | 自噬小体成核阶段是否顺利进行 | Western blot;免疫沉淀 | 用于证明某些蛋白/药物通过改写 Beclin 1 复合体调控自噬。[1,2] |
| ATG5–ATG12 共价复合物 | ATG5–ATG12 共轭条带 | 自噬小体延伸与 LC3 脂化过程中的组成部分 | Western blot | 更常用于机制研究;很多项目用 LC3/p62 + 通量对照即可覆盖核心问题。[1] |
| LC3-I → LC3-II 转换 | LC3-I 与 LC3-II 条带;LC3 puncta 斑点 | 自噬小体膜标记蛋白,是最常用 readout 之一 | Western blot;免疫荧光 / 共聚焦 | 单看 LC3-II 升高 ≠ 自噬增强。LC3 作为自噬膜标记的经典依据来自 LC3 处理与自噬体膜定位研究,通量解释建议以指南为准。[1,4] |
| p62 / SQSTM1 水平 | p62 总蛋白;p62 puncta 斑点 | 货物受体:通量顺畅时倾向下降;自噬受阻时累积 | Western blot;免疫荧光 | 常用判读:LC3-II ↑ + p62 ↓ 更支持“通量增加”;LC3-II ↑ + p62 ↑ 多提示“降解端堵车”。p62 与 LC3 直接结合并参与选择性自噬的证据来自经典研究。[1,5] |
| WIPI2 / early autophagosome | WIPI2 puncta 数量 | 早期自噬小体形成的 PI3P 结合蛋白 readout | 免疫荧光 | 适合精细时序:帮助区分“成核阶段问题”还是“融合/降解阶段问题”。[1] |
| 溶酶体标记 | LAMP1/LAMP2;LysoTracker 染色 | 自噬小体是否有足够溶酶体去融合并降解 | Western blot;免疫荧光;流式细胞术 | 在 chloroquine(氯喹)、bafilomycin A1(巴佛洛霉素 A1)等“抑制降解端”的实验里非常关键。[1,2] |
| 自噬通量报告构建 | 双荧光 LC3(区分自噬小体与自噬溶酶体) | 把“数量变化”和“通量变化”拆开看 | 荧光显微;高内涵成像 | 建议以指南的判读逻辑为主:必须配合“± 降解端抑制剂”条件来落地结论。[1] |
| 器官特异自噬(以线粒体自噬为例) | PINK1/Parkin 富集;线粒体蛋白(TOM20/COX IV)变化 | 特定细胞器是否通过自噬被选择性清除 | Western blot;免疫荧光 | 在神经退行性疾病、缺血再灌注等课题常见;Parkin 介导受损线粒体自噬的经典证据可参考代表性论文。[6] |
绝大多数自噬相关实验,最后都会落到一个问题:是自噬被激活了,还是被堵住了? 因此 panel 设计建议围绕有无降解端抑制剂 + LC3-II + p62 + 形态学证据来组合,而不是只看一条 LC3-II 条带。
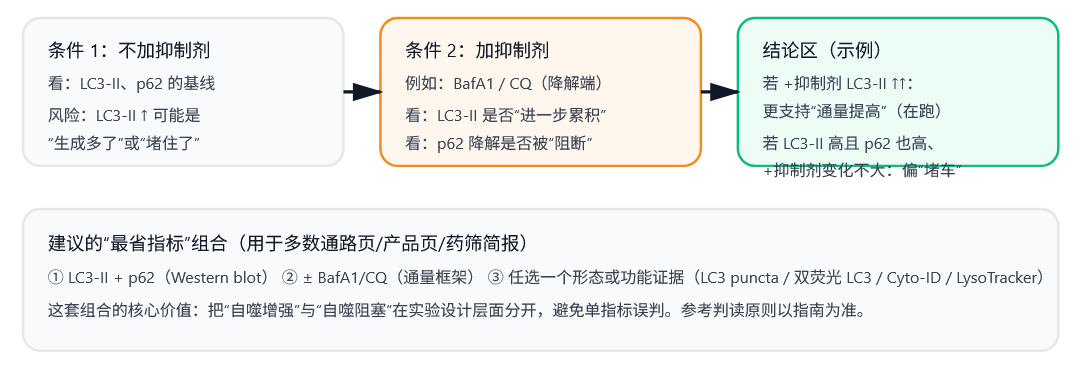
图2. 自噬通量的“可交付判读”:把 LC3-II 与 p62 放进“± 降解端抑制剂(例如 bafilomycin A1、chloroquine)”框架中看,优先避免单指标误判。
| 指标类型 |
Western blot (条带/裂解/比值) |
免疫荧光/共聚焦 (puncta/定位) |
流式细胞术 (单细胞定量) |
功能/通量框架 (± 抑制剂/读数) |
|
启动/上游 p-ULK1、Beclin 1 复合体 |
? | (可选) | (作为解释项) | |
|
形成 LC3-II、LC3 puncta |
? | ? | (可选) | 必须配合通量判断 |
|
通量/降解 p62、溶酶体 |
? | ? | ? | ? |
|
器官特异自噬 PINK1/Parkin、线粒体蛋白 |
? | ? | (可选) | 与通量框架联用更稳 |
如果只想用最少的指标覆盖自噬通路,建议优先考虑:
加上本篇,你的信号通路指标库在“代谢–应激–命运”模块又补上了一个重要拼图:自噬。 后续在专题页中,我们将继续分享 PI3K/AKT–mTOR、AMPK、自噬、凋亡几篇串成一条“能量感应–自噬–生死决策”的路线。
1、Klionsky DJ, Abdel-Aziz AK, et al. Guidelines for the use and interpretation of assays for monitoring autophagy (3rd edition). Autophagy. 2016. doi:10.1080/15548627.2015.1100356.
2、Mizushima N, Yoshimori T, Levine B. Methods in mammalian autophagy research. Cell. 2010. doi:10.1016/j.cell.2010.01.028.
3、Kim J, Kundu M, Viollet B, Guan KL. AMPK and mTOR regulate autophagy through direct phosphorylation of Ulk1. Nature Cell Biology. 2011. doi:10.1038/ncb2152. :contentReference[oaicite:0]{index=0}
4、Kabeya Y, Mizushima N, Ueno T, et al. LC3, a mammalian homologue of yeast Atg8, is localized in autophagosome membranes after processing. The EMBO Journal. 2000. doi:10.1093/emboj/19.21.5720. :contentReference[oaicite:1]{index=1}
5、Pankiv S, Clausen TH, Lamark T, et al. p62/SQSTM1 binds directly to Atg8/LC3 to facilitate degradation of ubiquitinated protein aggregates by autophagy. Journal of Biological Chemistry. 2007. doi:10.1074/jbc.M702824200. :contentReference[oaicite:2]{index=2}
6、Narendra D, Tanaka A, Suen DF, Youle RJ. Parkin is recruited selectively to impaired mitochondria and promotes their autophagy. Journal of Cell Biology. 2008. doi:10.1083/jcb.200809125.
返回顶部