
2025年美国已出现多起单核细胞增生李斯特菌(Lm,Listeria monocytogenes)食源性爆发事件,引发公共卫生领域的持续关注。2026年2月,美国FDA发布I级食品召回通报,俄勒冈马铃薯公司生产的近5.6万磅冷冻蓝莓因存在Lm污染风险启动召回,涉事大宗工业包装产品已销往美国密歇根、俄勒冈、华盛顿、威斯康星四州及加拿大。作为可在4℃常规冷藏环境下稳定增殖的高致病性食源性胞内寄生菌,Lm始终是全球冷链食品安全的核心防控对象,同时也是微生物学、感染免疫学领域研究胞内寄生菌-宿主互作的经典模式生物。

Lm为革兰氏阳性兼性厌氧短杆菌,是李斯特菌属中对人类致病性最强的人兽共患病原菌,无芽孢、无荚膜,运动能力具有显著温度依赖性:20-25℃可形成周生鞭毛表现活跃运动性,37℃宿主体温下鞭毛合成受抑、运动能力显著减弱。其最核心的生理特征为嗜冷性,可在0-45℃宽温区、pH 4.5-9.0酸碱环境中生长,4℃常规冷藏条件下仍能缓慢增殖,还可在食品加工设备表面形成生物膜,耐受消毒剂与环境胁迫,是冷链食品污染的核心致病菌。
基于菌体O/H抗原差异,Lm可分为13个血清型,血清型1/2a是全球食品污染分离株、临床感染株中占比最高的优势流行型别,也是目前实验室开展Lm基础研究最核心的模式菌株。其细胞壁以厚层肽聚糖为骨架,锚定大量毒力相关功能蛋白,其中IAP/p60是Lm特异性保守表达的肽聚糖水解酶,仅在致病性李斯特菌中稳定存在,既参与菌体形态维持与细胞壁重塑,也与毒力表型直接相关,是区分致病性与非致病性李斯特菌的核心标志物。
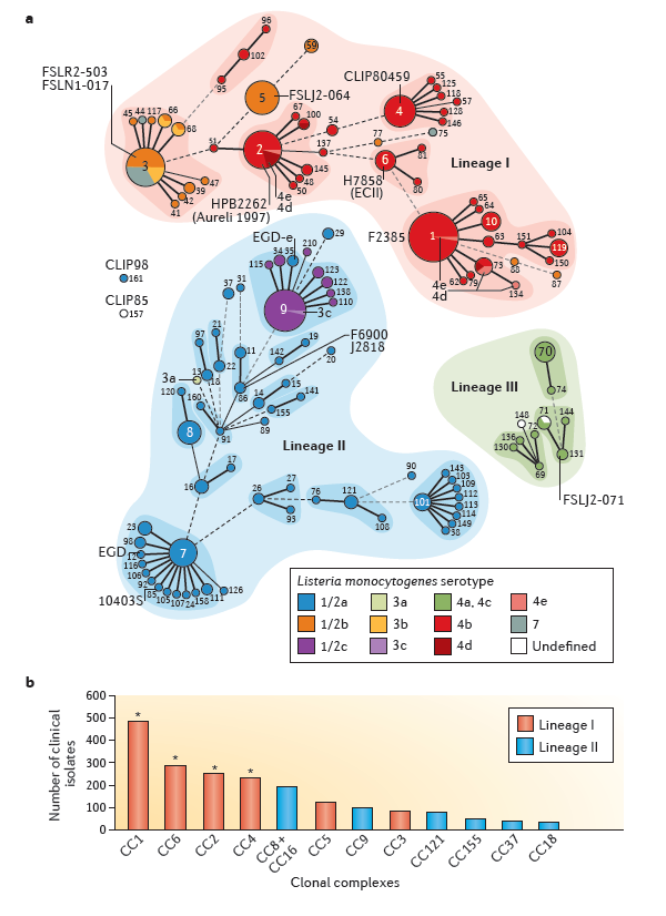
Figure 1: Listeria phylogeny
Lm广泛分布于土壤、水体、畜禽肠道等自然环境,可通过种植、加工、储运全链条污染食品,冷冻生鲜、即食乳制品等冷链品类为高风险对象。其感染为全球性食源性疾病,夏秋季为发病高峰,妊娠女性、老年人、免疫低下人群为侵袭性感染高危群体,此类人群感染病死率达20%~30%,全球超90%的临床感染病例由1/2a、4b血清型菌株引发。
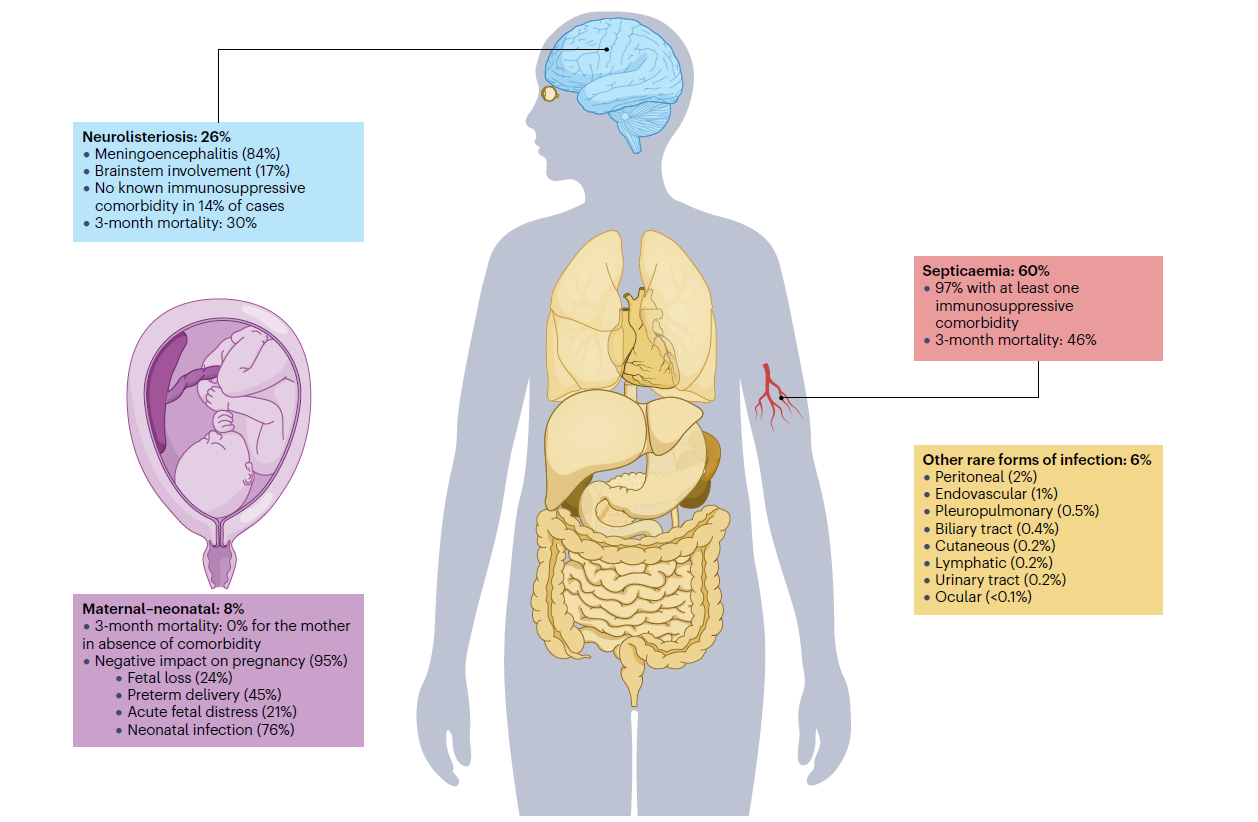
Figure 2: Clinical presentation and features of listeriosis

Lm的高致病性源于其完善的兼性胞内寄生循环,可通过一系列毒力因子的协同作用,完成宿主细胞黏附与入侵、吞噬体逃逸、胞内增殖、细胞间传播的全过程,同时高效逃避宿主免疫应答,最终突破肠道、血脑、胎盘等生理屏障,引发侵袭性感染。其绝大多数核心毒力基因位于李斯特菌毒力岛1(LIPI-1)上,表达受PrfA(阳性调控因子A)精准调控,形成了高度有序的毒力表达网络。
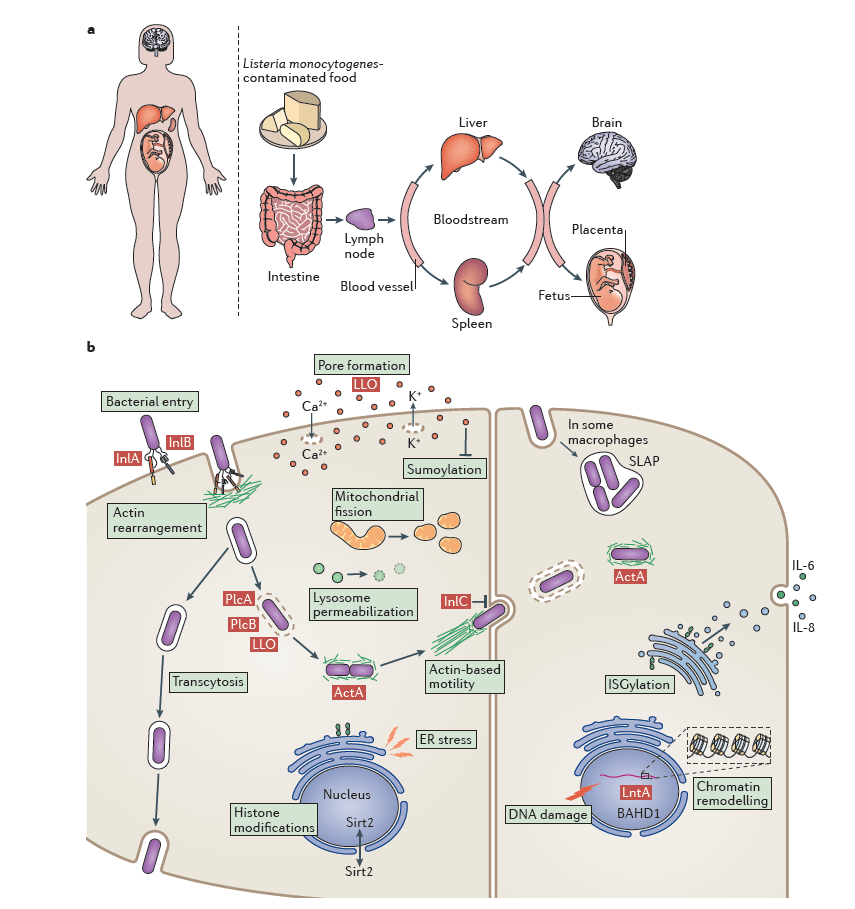
Figure 3: Overview of Listeria monocytogenes infection
黏附与入侵是Lm实现胞内寄生的起始步骤,该菌可主动侵袭宿主肠上皮细胞、肝细胞、胎盘滋养层细胞、脑微血管内皮细胞等非吞噬细胞,核心由内化素家族的InlA与InlB介导。InlA通过其亮氨酸富集重复序列结构域,特异性结合宿主上皮细胞表面的E-钙粘蛋白,启动菌体黏附与内化,是Lm突破肠道屏障的核心分子;InlB可特异性结合宿主肝细胞生长因子受体Met,激活PI3K-Akt信号通路诱导细胞骨架重排,辅助完成细菌入侵,同时参与Lm对血脑屏障、胎盘屏障的穿透。二者协同作用,为Lm实现宿主细胞定植奠定了关键基础
Lm被宿主细胞内吞进入吞噬体后,需快速裂解吞噬体膜逃逸至细胞质,才能避免被溶酶体降解,这是其实现胞内寄生的关键步骤,由李斯特菌溶血素O(LLO,由hly基因编码)与磷脂酶PlcA、PlcB协同完成。LLO属于胆固醇依赖型细胞溶素,在吞噬体酸性环境下被激活,可在膜上形成孔道破坏膜完整性;PlcA与PlcB通过水解细胞膜磷脂,与LLO协同增强裂解效率。hly基因缺失的Lm菌株会完全丧失胞内寄生能力与致病性,因此LLO是Lm最核心的毒力因子。
成功逃逸至宿主细胞质后,Lm可利用宿主细胞的营养物质快速增殖,同时通过actA基因编码的ActA蛋白劫持宿主肌动蛋白细胞骨架系统。ActA定位于菌体一端,可结合宿主Arp2/3复合物激活肌动蛋白聚合,在菌体尾部形成肌动蛋白彗星尾,推动细菌在胞内快速运动,并向相邻细胞膜形成膜突起,被相邻细胞内吞后实现细胞间传播。该过程全程不暴露于胞外环境,可彻底逃避宿主体液免疫的杀伤,是Lm实现持续性感染的核心环节。
Lm突破肠道上皮屏障后,可经血液循环播散至肝、脾等网状内皮系统器官,进一步穿透血脑屏障引发中枢神经系统感染,突破胎盘屏障造成流产、早产、新生儿败血症等严重临床结局。该过程仍依赖InlA、InlB、LLO、ActA等核心毒力因子的协同作用,同时菌株的毒力表型、宿主免疫状态直接决定感染的严重程度。
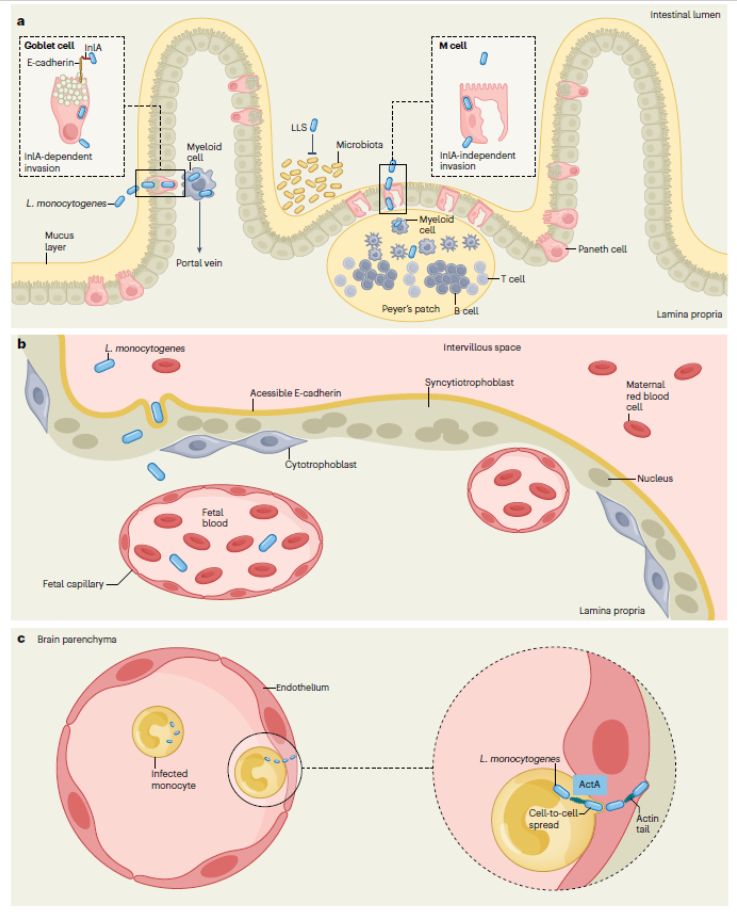
Figure 4: Mechanisms by which L. monocytogenes crosses host barriers

Lm既是全球食品安全领域重点防控的致病菌,也是微生物学、细胞生物学、感染免疫学与转化医学领域的重要模式生物,其核心研究方向覆盖基础机制解析、应用技术研发与转化医学应用多个维度,为食品安全防控、感染性疾病治疗及肿瘤免疫研究提供重要支撑。
快速、精准的检测与溯源是Lm食品安全防控与临床诊断的核心基础,相关研究主要分为通用型检测与分型溯源两大方向。通用型检测以Lm特异性保守基因与蛋白为靶点,开发高特异性的核酸检测与免疫学检测方法,实现对致病性Lm的快速筛查;分型溯源则以血清型鉴定、全基因组测序、多位点序列分型为核心,完成菌株亲缘关系鉴定与传播链分析,为疫情处置提供精准依据。
主要包括:毒力因子功能解析、PrfA核心调控网络、宿主模式识别与免疫应答机制、胞内寄生的细胞生物学基础。Lm作为经典的胞内寄生模式菌,其研究成果不仅完善了食源性致病菌的致病理论,也为胞内病原体的宿主互作研究提供了通用范式。
Lm的防控技术研究主要分为三大方向:食品加工环节的抑菌与生物膜清除技术、环境消毒技术、宿主感染的疫苗研发。食品防控技术主要针对Lm的嗜冷性与生物膜形成能力,研发新型抑菌剂、天然抗菌物质、消毒剂与生物膜清除方案,从加工全链条降低污染风险;疫苗研发则围绕Lm的核心毒力抗原展开,旨在诱导宿主产生高效的保护性免疫应答,重点面向妊娠女性、老年人等高危群体。
Lm凭借其高效的胞内寄生能力与免疫激活特性,被广泛改造为肿瘤免疫治疗的疫苗载体,是合成生物学与转化医学领域的研究热点。相关研究通过敲除毒力基因构建减毒菌株,同时表达肿瘤相关抗原与细胞因子,可在体内高效激活抗原递呈细胞,诱导抗肿瘤特异性CD8+ T细胞免疫应答,目前已有多项Lm载体肿瘤疫苗进入临床试验阶段。

abinScience创立于法国,专注于高质量生命科学试剂的开发与生产,立足法国斯特拉斯堡创新科技中心,以“Empowering Bioscience Discovery”为愿景。
| Product Name | Catalog No. |
| Anti-Listeria monocytogenes serovar 1/2a InlB/Internalin B Antibody (SAA0363) | JN937013 |
| Anti-Listeria monocytogenes serovar 1/2a IAP Monoclonal Antibody (1A180) | JN846025 |
| Anti-Listeria monocytogenes serotype 1/2a InlB/Internalin B Nanobody (SAA0997) | JN937023 |
| Recombinant Listeria monocytogenes IAP/p60 Protein, N-His | JN846012 |
更多关于李斯特菌相关研究产品欢迎扫码咨询或发邮件给我们:support@abinscience.com

[1] Lecuit M. Listeria monocytogenes, a model in infection biology. Cell Microbiol. 2020 Apr;22(4):e13186. doi: 10.1111/cmi.13186. PMID: 32185900.
[2] Disson
O, Moura A, Lecuit M. Making Sense of the Biodiversity and Virulence of
Listeria monocytogenes. Trends Microbiol. 2021 Sep;29(9):811-822. doi:
10.1016/j.tim.2021.01.008. Epub 2021 Feb 11. PMID: 33583696.
[3] Meireles
D, Pombinho R, Cabanes D. Signals behind Listeria monocytogenes
virulence mechanisms. Gut Microbes. 2024 Jan-Dec;16(1):2369564. doi:
10.1080/19490976.2024.2369564. Epub 2024 Jul 9. PMID: 38979800; PMCID:
PMC11236296.
[4] Jordan
K, McAuliffe O. Listeria monocytogenes in Foods. Adv Food Nutr Res.
2018;86:181-213. doi: 10.1016/bs.afnr.2018.02.006. Epub 2018 Apr 3.
PMID: 30077222.
[5] Lopes-Luz
L, Mendon?a M, Bernardes Foga?a M, Kipnis A, Bhunia AK, Bührer-Sékula
S. Listeria monocytogenes: review of pathogenesis and virulence
determinants-targeted immunological assays. Crit Rev Microbiol. 2021
Sep;47(5):647-666. doi: 10.1080/1040841X.2021.1911930. Epub 2021 Apr 24.
PMID: 33896354.
[6] Radoshevich
L, Cossart P. Listeria monocytogenes: towards a complete picture of its
physiology and pathogenesis. Nat Rev Microbiol. 2018 Jan;16(1):32-46.
doi: 10.1038/nrmicro.2017.126. Epub 2017 Nov 27. PMID: 29176582.
[7] Disson
O, Charlier C, Pérot P, Leclercq A, Paz RN, Kathariou S, Tsai YH,
Lecuit M. Listeriosis. Nat Rev Dis Primers. 2025 Oct 2;11(1):71. doi:
10.1038/s41572-025-00654-x. PMID: 41038831.
返回顶部