
流式实验结果的准确性不仅取决于抗体选择和仪器设置,样本本身的状态同样至关重要。死细胞由于其膜通透性变化,常会导致抗体非特异性结合;同时死细胞还会导致细胞自发荧光增强,从而引入假阳性信号并模糊细胞群的分界。这种干扰在检测稀有细胞群或低表达抗原时尤为显著。
死细胞膜完整性受损后,胞内大量带电荷的组分及非特异性抗原表位暴露,会与荧光标记抗体发生非特异性吸附,导致假阳性信号的产生。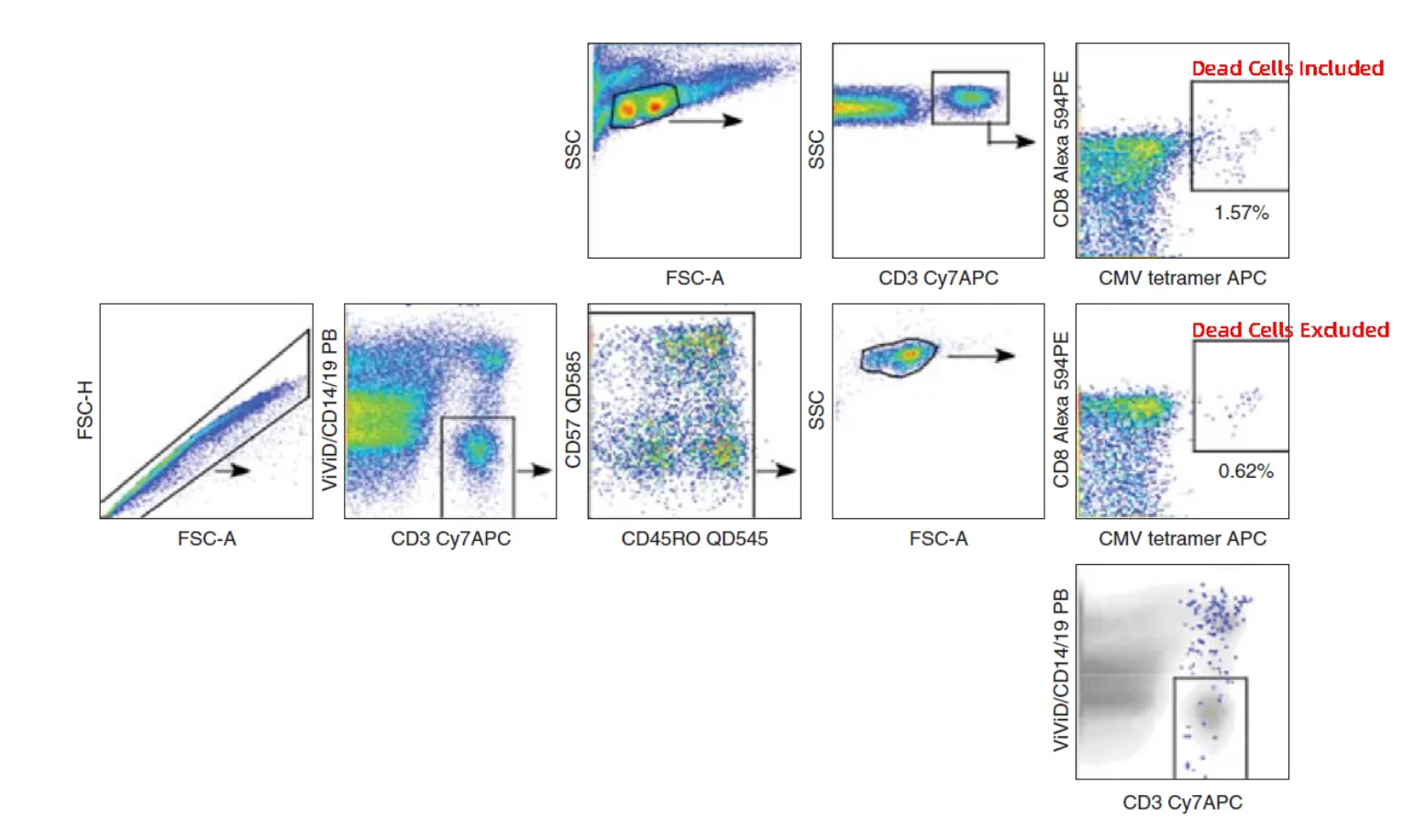
图1. 死细胞导致假阳性信号
细胞死亡过程中,线粒体、溶酶体等细胞器释放的代谢产物(如黄素类、脂褐素)可显著增强细胞的自发荧光。这种自发荧光具有宽谱特性,可溢漏至多个检测通道,导致背景信号升高。在有些实验结果中会表现为沿对角线分布的信号。这也是识别死细胞干扰的一个重要特征。
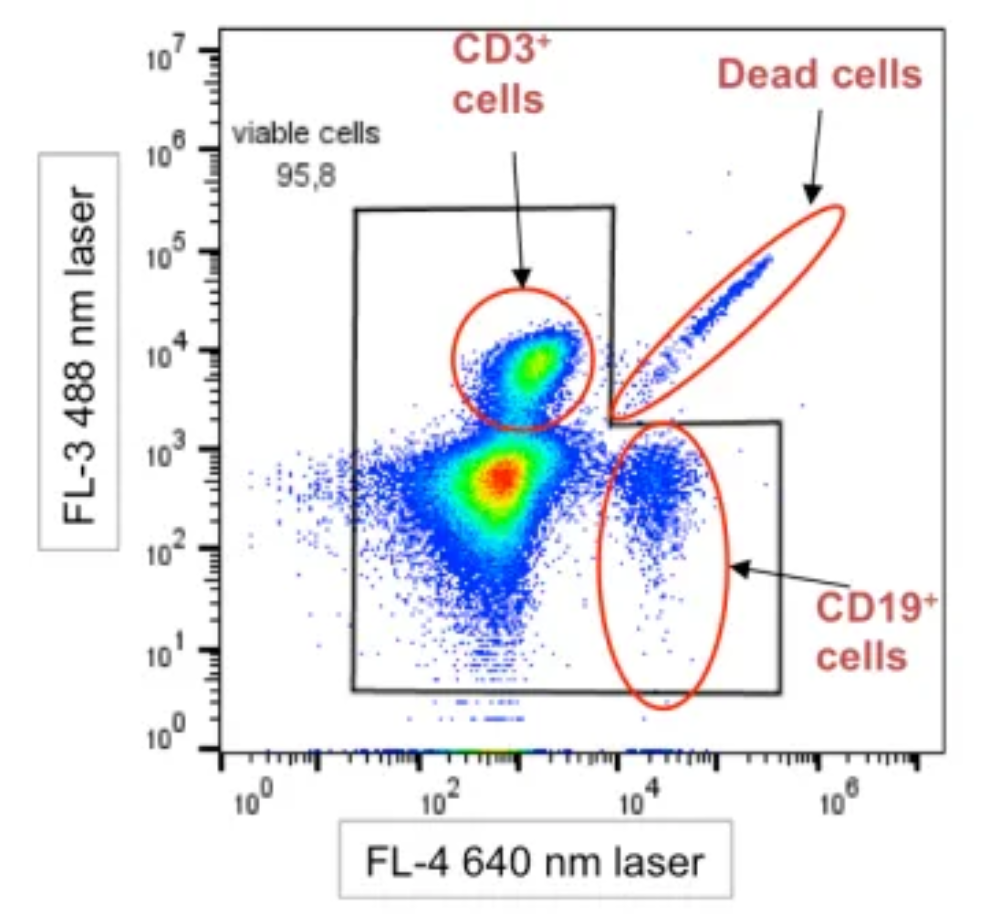
图2. 死细胞沿对角线分布示意图
上述两种效应叠加,会导致目标细胞群在散点图上呈现斜向拖尾或与边界不清,影响圈门的准确性和可重复性,尤其在检测稀有细胞或弱表达抗原时,可能造成细胞漏检或误计。
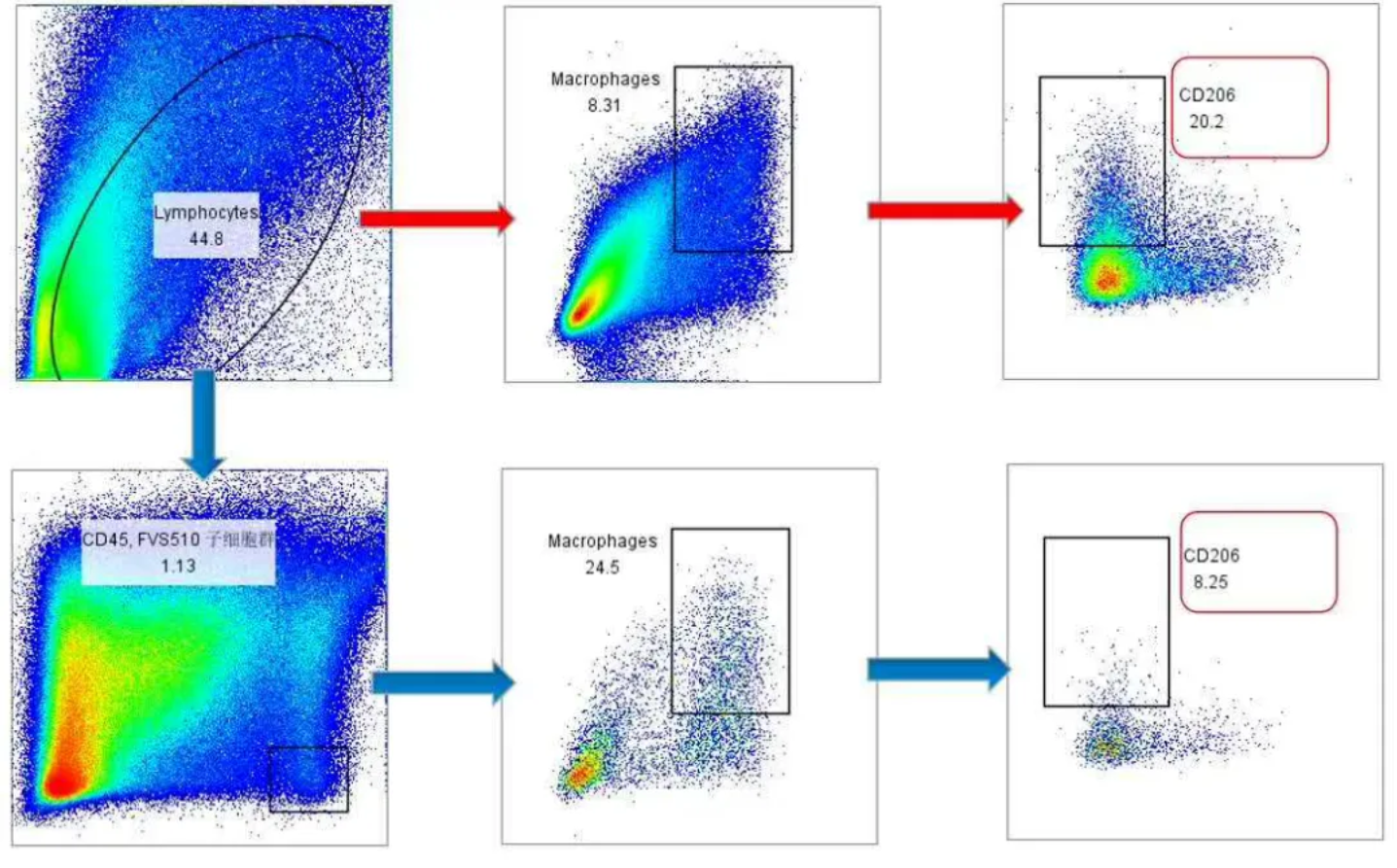
图3. 未染死活和CD45导致CD11b+F4/80+的巨噬细胞群分群不清晰及CD206异常升高
常用死活染料可根据实验需求分为两类:
核酸染料基于细胞膜完整性:活细胞能够排斥染料,而死细胞膜破损后,染料进入细胞并与DNA结合,产生荧光。此类染料适用于不涉及固定破膜的样本直接检测。细胞在固定处理后,细胞膜通透性改变,染料会进入活细胞,导致无法区分死活。
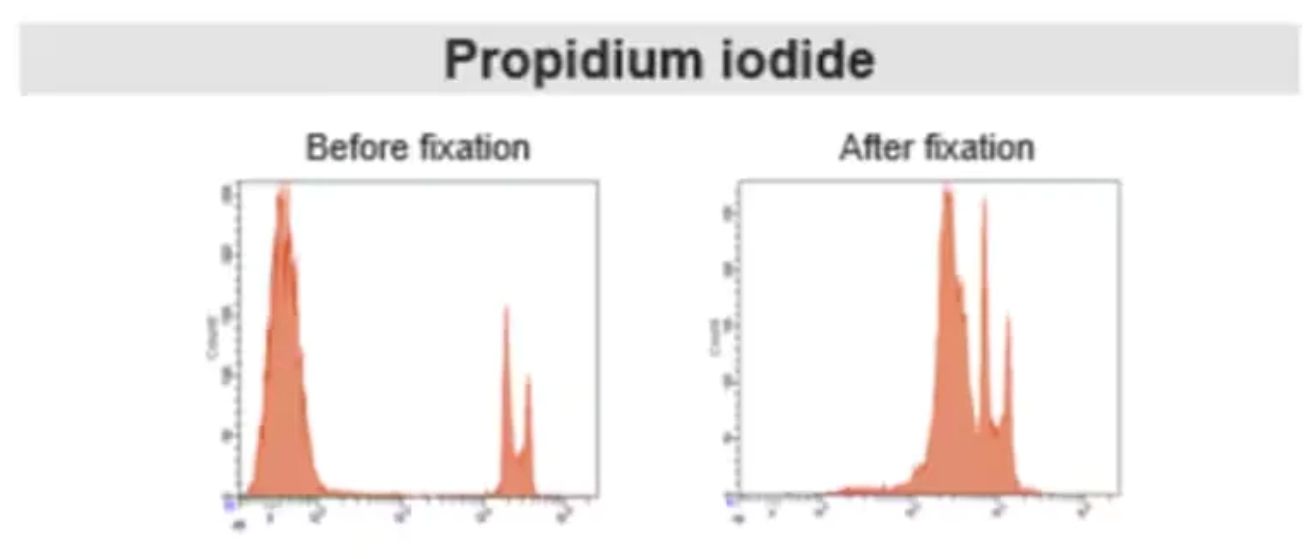
图4. 固定前后PI染色结果对比
胺基活性染料通过共价结合蛋白质标记细胞。细胞膜破损后,染料进入死细胞内标记大量蛋白质,使荧光强度明显高于仅标记膜表面蛋白的活细胞。此类染料能够耐受后续的固定和破膜处理,适用于需要胞内染色的复杂实验方案。
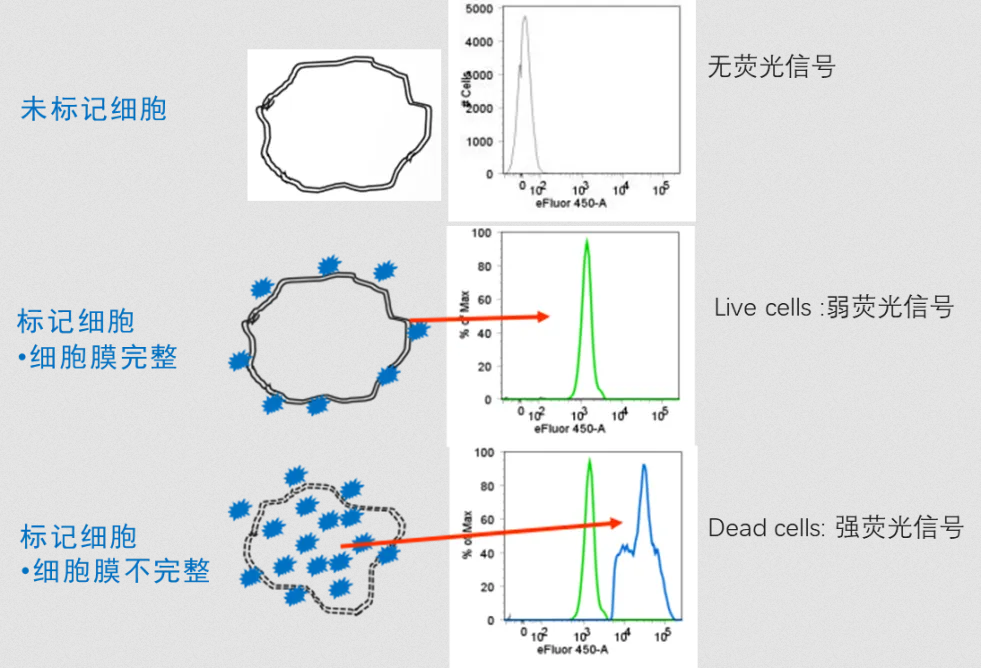
图5. 胺基活性染料区分死活细胞原理
在实验设计阶段,应首先确认是否需要固定或破膜处理,从而选择合适的染料类型。
| 死活染料类型 | 核酸类死活染料 | 胺基活性染料 |
| 染色原理 | 细胞膜非通透性核酸染料,可进入细胞膜受损的细胞并与dsDNA/RNA结合,但不能穿透完整细胞膜。 | 细胞膜非通透性胺基活性染料,与位于细胞内外的细胞蛋白上的伯胺基团共价结合。只与细胞表面的氨基蛋白结合时,仅产生微弱的信号;然而,当染料通过受损的质膜进入细胞并与细胞内部的氨基蛋白反应时,产生的信号非常强。 |
| 染色顺序 | 表染后,上机前 | 表染前 |
| 是否可染色后固定 | 否 | 是 |
| 荧光颜色选择 | 少,配色受限 | 多,灵活配色 |
| 常见染料 | PI, 7AAD, DAPI | Invitrogen? LIVE/DEAD可固定死细胞染色剂,eBioscience? Fixable Viability Dye(即用型细胞活性判断染料,可用于胞内染色的死活染料) |
| 其他特点 | 发射波谱比较宽,与其他通道干扰较大;占用较好的通道;PI等染料黏性大;不可用于需固定细胞的流式检测。 | 有多种荧光标记可以选择,灵活加入配色panel;避免细胞容易成团的问题,不易堵塞流式仪器管路。 |
胺基染料也是需要通过梯度滴定确定最佳工作浓度,目标是实现活细胞与死细胞的最大分离度(Stain Index),而非单纯追求荧光强度。浓度过高会提高活细胞背景,过低则无法充分标记死细胞。对新批次染料,应进行滴定实验以保证一致性。
胺基染料结合蛋白质,高浓度蛋白(如血清、BSA)会竞争染料结合,削弱阳性信号。因此,染色应在不含蛋白的缓冲液(如PBS)中进行,完成后再使用含蛋白缓冲液洗涤封闭。
在设计多参数panel时,应考虑死活染料通道可能对其他检测通道造成的信号扩散(Spreading Error)。合理安排染料组合有助于减少弱表达抗原检测的干扰。
死活染色是流式实验质控的关键环节。通过合理选择染料类型、滴定确定最佳浓度,并严格控制染色条件,可以有效排除死细胞干扰,提高实验数据的准确性与可重复性,也为科学结论提供可靠基础。
abinScience创立于法国,专注于高质量生命科学试剂的开发与生产,致力于为科研工作者提供高性能、高可靠性的流式抗体。针对T细胞亚群、免疫检查点、记忆/耗竭标志物等研究,我们可提供:
1. 经过严格验证的CD3、CD4、CD8等流式抗体,确保高灵敏度与低背景;
2. 覆盖Human、Mouse、Rat、Dog、Hamster等多物种的免疫学研究工具;
3. 专业的技术支持与Panel设计咨询,助您精准解析复杂免疫细胞群体。
更多abinScience流式抗体信息请点击:
查看abinScience流式抗体
[1]
Perfetto SP, Chattopadhyay PK, Lamoreaux L, Nguyen R, Ambrozak D, Koup
RA, Roederer M. Amine-reactive dyes for dead cell discrimination in
fixed samples. Curr Protoc Cytom. 2010 Jul;Chapter 9:Unit 9.34. doi:
10.1002/0471142956.cy0934s53. PMID: 20578108; PMCID: PMC2915540.
[2]
Perfetto SP, Chattopadhyay PK, Lamoreaux L, Nguyen R, Ambrozak D, Koup
RA, Roederer M. Amine reactive dyes: an effective tool to discriminate
live and dead cells in polychromatic flow cytometry. J Immunol Methods.
2006 Jun 30;313(1-2):199-208. doi: 10.1016/j.jim.2006.04.007. Epub 2006
May 19. PMID: 16756987.
返回顶部