
近期,我国首次发生输入性南非1型(SAT1)口蹄疫疫情,该血清型为非洲特有毒株,与我国长期流行的O型、A型、亚洲1型等毒株在基因组、衣壳结构、抗原蛋白组成及表位构象上存在本质区别,不同血清型间无交叉免疫保护,现有常规疫苗无法提供有效保护。
口蹄疫病毒属于小RNA病毒科口蹄疫病毒属,为无囊膜二十面体对称病毒,直径约25–30nm,基因组为单股正链RNA,全长约8.5kb,编码一个开放阅读框,经蛋白酶切割后产生结构蛋白与非结构蛋白。FMDV存在7种主要血清型(O、A、C、Asia 1、SAT1-3)及众多亚型,不同血清型间无交叉免疫保护,且病毒RNA复制过程易发生突变,导致新变异株持续出现,这也是传统疫苗防控的主要障碍。
SAT1型与O、A、Asia1型在基因组组织形式上一致,均由5’UTR?L?P1?P2?P3?3’UTR?poly(A)组成,其中P1区编码VP1、VP2、VP3、VP4四种结构蛋白,共同构成病毒衣壳;P2、P3区编码Lpro、2A、2B、2C、3A、3B、3Cpro、3Dpol等非结构蛋白,参与病毒复制、蛋白加工及免疫逃逸过程。
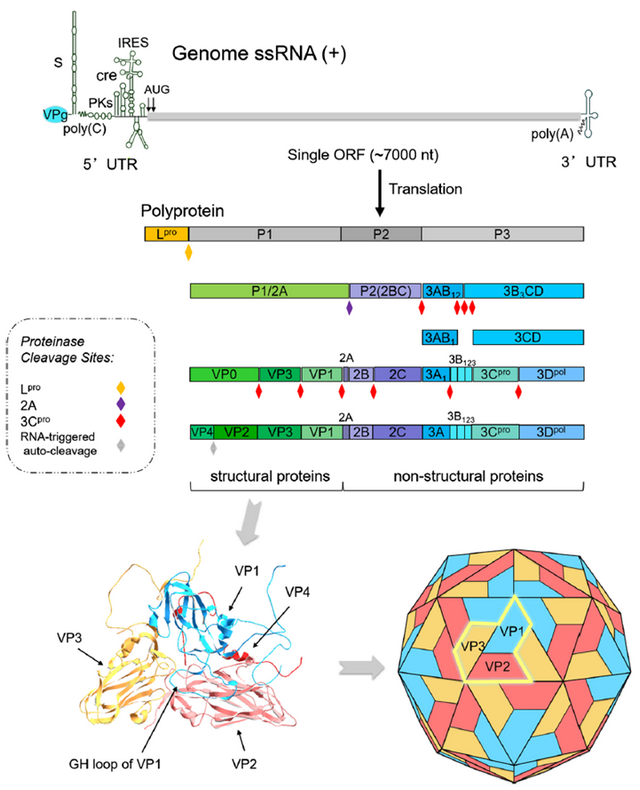
Figure 1. 口蹄疫病毒(FMDV)基因组、病毒多肽加工及结构蛋白构象
在结构蛋白层面,VP1、VP2、VP3暴露于病毒粒子表面,是诱导中和抗体的主要抗原,VP4位于衣壳内部,不参与抗原识别。VP1是决定血清型特异性的核心蛋白,其G?H环与C端为主要中和表位区域,SAT1型与普通流行株在VP1编码区核苷酸与氨基酸序列差异超过40%,这是血清型特异性与无交叉保护的分子基础。普通流行株的VP1 G?H环序列相对保守,与现有疫苗抗原高度匹配,可诱导特异性中和抗体;而SAT1型VP1 G?H环为高变区,氨基酸替换集中,构象显著改变,且存在特有二硫键稳定局部结构,导致原有疫苗诱导的抗体无法识别。尽管SAT1型VP1仍保留高度保守的RGD基序,可通过结合宿主细胞 αvβ6整合素介导入侵,但其表面环区额外携带正电荷氨基酸,可利用硫酸乙酰肝素等辅助受体入侵,细胞结合效率与组织嗜性更强。VP2与VP3在SAT1型中同样存在关键氨基酸替换,B?C环、E?F环等区域序列变异,导致构象依赖性抗原表位重塑,与 O、A、Asia1型抗体无交叉反应。VP4在各血清型中高度保守,位于衣壳内部,不诱导保护性中和抗体,无血清型特异性差异。
SAT1型与普通流行株的非结构蛋白整体同源性较高,但抗原性存在差异。Lpro与3Cpro可通过切割宿主eIF4G、RIG?I/MDA5等分子抑制I型干扰素通路,3Dpol为RNA依赖的RNA聚合酶,负责基因组复制,3A参与膜重排与宿主范围调控。在检测应用中,3ABC抗体检测策略可有效区分自然感染动物与灭活疫苗免疫动物,该方法不受SAT1与普通血清型差异影响,具备通用性。
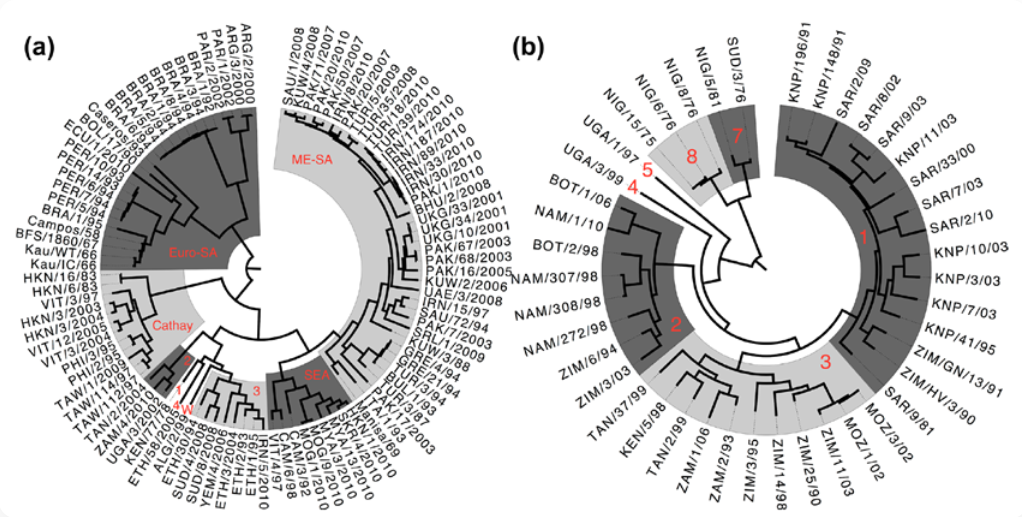
Figure 2. O型和SAT1型血清群的系统发育树
从结构与抗原角度看,SAT1型与普通流行株的核心差异集中于衣壳表面抗原表位的序列与构象,尤其是VP1 G?H环的高变异与特有二硫键,直接导致常规疫苗抗体无法中和SAT1病毒。各血清型间完全无交叉免疫保护,是口蹄疫防控中必须分型免疫、使用专用疫苗的根本原因。SAT1型作为外来输入毒株,我国畜禽群体无免疫基础,其传播效率高、幼畜致死率高、临床损伤更严重,对养殖业构成重大威胁。
FMDV是已知传染性最强的动物病毒之一,其基本再生数(R?)在牛群中可达2.52-14,小型实验中甚至出现无限传播的极端情况。病毒主要通过直接接触、呼吸道飞沫及污染物传播,侵入宿主后首先在口腔黏膜、蹄部上皮细胞中复制,随后通过血液循环扩散至全身。
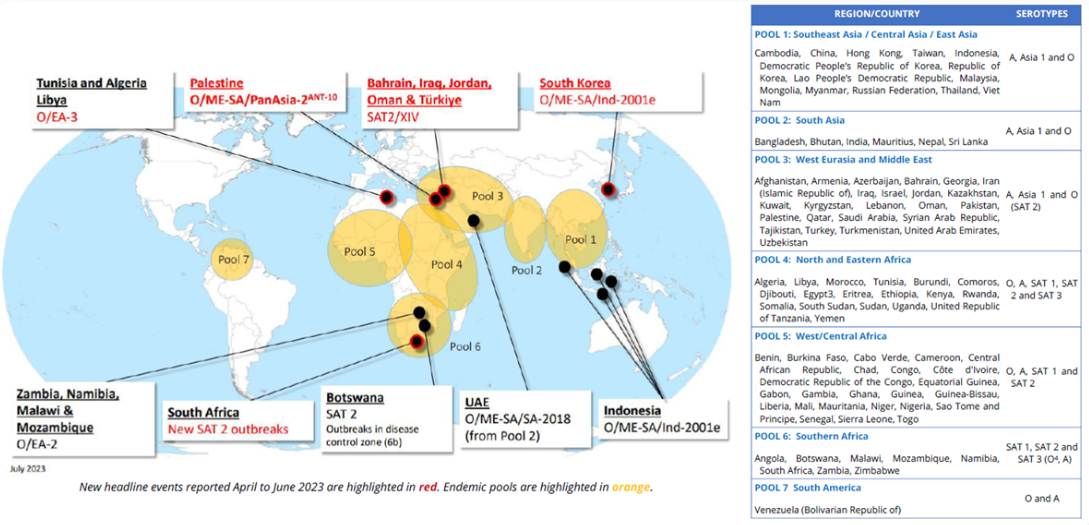
Figure 3. FMD的地理分布和最近全球爆发情况
致病过程中,FMDV的VP1蛋白与宿主细胞表面的整合素αvβ6结合,介导病毒内化,其复制会导致上皮细胞坏死脱落,形成特征性的口腔水疱、蹄部溃烂症状。虽然成年动物死亡率较低,但会引发严重的生产损失:泌乳奶牛产奶量下降20%-80%,育肥动物体重减轻10%-25%,繁殖动物流产率升高至28.8%,且感染动物的牵引能力丧失可持续20天以上。更严重的是,病毒可在非洲水牛等野生动物中持续存在,形成自然疫源地,给疫病根除带来巨大挑战。
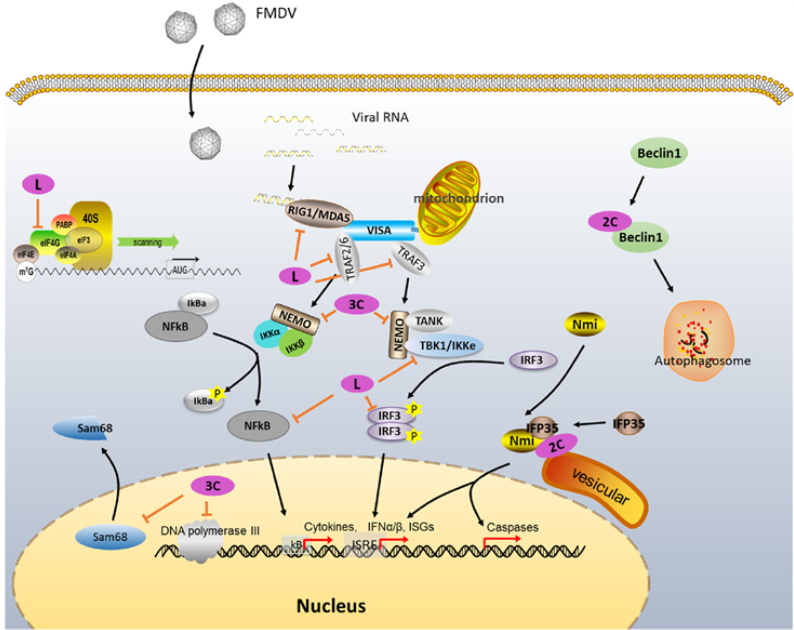
Figure 4. FMDV非结构蛋白在细胞调控中的已知功能
基于结构生物学与病原进化研究证实,SAT1型口蹄疫病毒VP1 G?H环高变异、特有二硫键构象及表面抗原表位重塑是其与O/A/Asia1型无交叉保护的核心分子机制,相关成果已发表于Veterinary Research等权威期刊,为精准疫苗设计提供关键依据。
国际上,针对SAT1的商用疫苗已在非洲、中东广泛应用,包括Bioaftogen®(阿根廷 Biogénesis Bagó公司,SAT1/SAT2 多价灭活疫苗)、Aftovaxpur DOE(勃林格殷格翰,含 SAT1/SAT2组分)、摩洛哥Biopharma四价疫苗(O+A+SAT1+SAT2)等,均通过WOAH标准效力验证,在牛群中可诱导稳定中和抗体,满足区域防控需求。
我国在SAT1首次输入后快速启动应急研发,农业农村部先后批准中农威特生物科技股份有限公司(2026?04?01)、金宇保灵生物药品有限公司(生物股份子公司)(2026?04?05)生产两款应急疫苗,分别为口蹄疫南非1型灭活疫苗(Re?SAT1/2026株)与口蹄疫南非1型亚单位疫苗,毒株源自我国分离鉴定的流行株,免疫原性与安全性通过临床试验验证,具备DIVA兼容、无散毒风险等优势,已投入疫区紧急免疫使用。同时,SAT1特异性荧光RT?PCR、ELISA检测试剂同步获批,形成分型检测与专用疫苗配套的精准防控体系。
以下为 abinScience 针对FMDV相关的重组蛋白与抗体产品,目录号可直接点击进入产品页。
| Catalog No. | Product name |
| VK164012 | Recombinant FMDV (SAT-1) VP2 Protein,N-His |
| VK164022 | Recombinant FMDV (SAT-1) VP3 Protein,N-His |
| VK164032 | Recombinant FMDV (SAT-1) VP4 Protein,N-His |
| VK164042 | Recombinant FMDV (SAT-1) Protease 3C,N-His |
| VK500122 | Recombinant FMDV VP0 Protein, N-His-KSI |
| VK500132 | Recombinant FMDV (SAT-1) VP1 Protein, N-His |
| VK500052 | Recombinant FMDV Lpro Protein, N-His |
| VK500062 | Recombinant FMDV VP2 Protein, N-His |
| VK500072 | Recombinant FMDV VP3 Protein, N-His |
| VK500082 | Recombinant FMDV VP1 Protein, N-His |
| Catalog No. | Product name |
| VK500134 | Anti-FMDV (SAT-1) VP1 Polyclonal Antibody |
| VK500124 | Anti-FMDV VP0 Polyclonal Antibody |
| VK500014 | Anti-FMDV Capsid protein VP1 Polyclonal Antibody |
| VK500013 | Anti-FMDV Capsid protein VP1 Antibody (SD6) |
| VK500023 | Anti-FMDV Capsid protein VP1 Antibody (4C4) |
| VK500033 | Anti-FMDV Capsid protein VP1 Antibody (4A2) |
| VK500043 | Anti-FMDV Capsid protein VP1 Antibody (1E12#) |
| VK500053 | Anti-FMDV Genome polyprotein Antibody (54#) |
| VK500063 | Anti-FMDV Genome polyprotein Antibody (201#) |
| VK657013 | Anti-Foot-and-mouth disease virus/FMDV 3ABC/3B Antibody (FM27) |
需要AIH研究工具?
abinScience提供原厂直供的自身免疫性肝炎相关重组蛋白、抗体及ELISA试剂盒,支持批量询价、定制规格及技术咨询。
技术咨询立即询价
联系邮箱:info@abinscience.com | 电话:027--87433958Reference:
1.
Dong H, Liu P, Bai M, et al. Structural and molecular basis for
foot-and-mouth disease virus neutralization by two potent protective
antibodies. Protein Cell. 2022;13(6):446-453.
doi:10.1007/s13238-021-00828-9
2. Park JY, Lee HM, Kang KJ, et al.
Development and immunogenicity of adenoviral Fc-fused FMDV virus-like
particle vaccine in swine. Vet Q. 2025;45(1):2564443.
doi:10.1080/01652176.2025.2564443
3. Kotecha A, Seago J, Scott K, et
al. Structure-based energetics of protein interfaces guides
foot-and-mouth disease virus vaccine design. Nat Struct Mol Biol.
2015;22(10):788-794. doi:10.1038/nsmb.3096
4. Porta C, Kotecha A,
Burman A, et al. Rational engineering of recombinant picornavirus
capsids to produce safe, protective vaccine antigen. PLoS Pathog.
2013;9(3):e1003255. doi:10.1371/journal.ppat.1003255
5. Sultanov AA,
Tyulegenov S, Yessembekova GN, et al. The progressive control of
foot-and-mouth disease (FMD) in the Republic of Kazakhstan: Successes
and challenges. Front Vet Sci. 2023;10:1036121. Published 2023 Apr 17.
doi:10.3389/fvets.2023.1036121
6. Li Y, Zeng W, Niu X, et al.
Foot-and-mouth disease virus-like particle vaccine incorporating
dominant T and B cell epitopes: enhanced immune response in piglets with
CD154 molecules. Front Vet Sci. 2025;12:1540102. Published 2025 Feb 19.
doi:10.3389/fvets.2025.1540102
7. Gao Y, Sun SQ, Guo HC. Biological
function of Foot-and-mouth disease virus non-structural proteins and
non-coding elements. Virol J. 2016;13:107. Published 2016 Jun 22.
doi:10.1186/s12985-016-0561-z
8. Stenfeldt C, Eschbaumer M, Humphreys
J, Medina GN, Arzt J. The pathogenesis of foot-and-mouth disease virus:
current understandings and knowledge gaps. Vet Res. 2025;56(1):119.
Published 2025 Jun 16. doi:10.1186/s13567-025-01545-5
9. Jiang S,
Yang S, Zhang X, et al. Evolutionary and structural insights into VP1
epitopes of representative SAT-type FMDV strains: implications for
candidate vaccine selection. Vet Res. 2025;56(1):227. Published 2025 Dec
15. doi:10.1186/s13567-025-01643-4
10. Elrashedy A, Mousa W, Nayel
M, et al. Systematic review and meta-analysis of the effectiveness of
polypeptide, virus-like particles, and viral vector vaccines for
foot-and-mouth disease (2020-2025). Sci Rep. 2025;15(1):39370. Published
2025 Nov 10. doi:10.1038/s41598-025-24078-5
11. Yu SC, Lee IK, Kong
HS, et al. Foot-and-Mouth Disease Virus-like Particles Produced in E.
coli as Potential Antigens for a Novel Vaccine. Vet Sci. 2025;12(6):539.
Published 2025 Jun 2. doi:10.3390/vetsci12060539
12. Reeve R, Borley
DW, Maree FF, Upadhyaya S, Lukhwareni A, Esterhuysen JJ, Harvey WT,
Blignaut B, Fry EE, Parida S, Paton DJ, Mahapatra M. Tracking the
Antigenic Evolution of Foot-and-Mouth Disease Virus. PLoS One. 2016 Jul
22;11(7):e0159360. doi: 10.1371/journal.pone.0159360. PMID: 27448206;
PMCID: PMC4957747.
返回顶部