
2026年3月3日,日本协和麒麟(Kyowa Kirin)发布官方公告,宣布立即终止OX40靶向单克隆抗体Rocatinlimab的全部全球临床试验。此前,该药物的全球合作开发方安进(Amgen),已于2026年2月以战略优先级调整为由,将Rocatinlimab的全球开发权全部退回协和麒麟。
作为全球推进至多项III期临床的OX40阻断型抗体,Rocatinlimab核心适应症覆盖中重度特应性皮炎、结节性痒疹、哮喘等自身免疫病,曾被行业视为该靶点最接近上市的重磅品种。协和麒麟在公告中明确终止核心依据:临床试验安全性审查中,发现新的免疫缺陷相关恶性肿瘤风险信号——在既往1例卡波西肉瘤病例基础上,新增1例确诊、1例疑似病例,累计3例相关不良事件。经联合评估,认定药物在目标人群中的潜在风险大于临床获益,因此全面终止所有临床试验。
卡波西肉瘤多见于免疫监视功能受损人群,这一信号并非简单的用药不良反应,而是直接指向OX40靶点领域的核心痛点:我们对OX40的基础生物学机制、免疫调控的安全边界,仍存在大量尚未填补的认知空白。
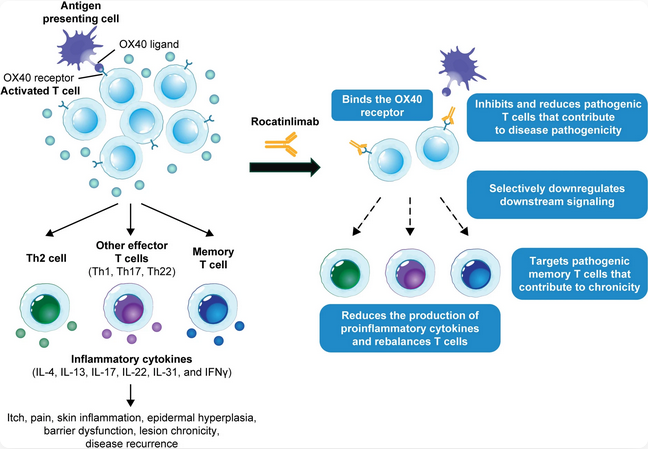
Figure 1. Rocatinlimab的作用机制
OX40又称CD134,编码基因为TNFRSF4,属于肿瘤坏死因子受体超家族(TNFRSF)成员,是T细胞活化过程中关键的晚期共刺激信号分子,直接决定机体免疫应答的强度、持续时间与稳态平衡。
人源OX40为I型跨膜糖蛋白,蛋白结构分为胞外区、跨膜区与胞内区三个核心部分:胞外区的富含半胱氨酸结构域是介导配体结合的核心区域,胞内区无内在激酶活性,通过招募TNF受体相关因子(TRAF)家族蛋白完成下游信号的传递。
OX40的表达具有严格的诱导性与细胞特异性,仅在免疫细胞活化后被诱导上调,这也是其与经典共刺激分子CD28最核心的区别。静息状态的T细胞不表达OX40,当T细胞经TCR与CD28共刺激完成初始活化后,OX40的表达会在24小时左右开始上调,48-72小时达到表达峰值,随后逐渐下降。其表达主要集中于活化的CD4+辅助性T细胞、CD8+细胞毒性T细胞、调节性T细胞(Treg)等T细胞谱系;病理状态下,肿瘤浸润淋巴细胞、自身免疫病病灶浸润的T细胞中,OX40会呈现显著高表达,且表达水平与T细胞活化状态密切相关。
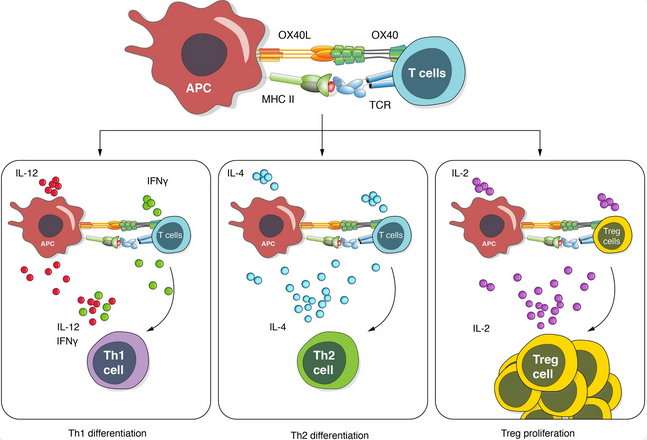
Figure 2. OX40/OX40L信号传导调节T细胞增殖和极化
OX40被激活后会启动多条下游核心信号通路,核心功能是维持T细胞的持续活化与长期存活,弥补CD28介导的早期共刺激信号的不足:通过上调抗凋亡蛋白延长活化T细胞的存活时间,避免活化诱导的细胞死亡;同时促进T细胞增殖,增强效应细胞因子分泌与细胞毒性功能。OX40在不同疾病领域呈现双向转化潜力:在肿瘤免疫领域,激动型抗体可显著增强抗肿瘤活性、逆转T细胞耗竭,与PD-1/PD-L1抑制剂具有显著协同效应;在自身免疫性疾病领域,OX40信号过度活化会驱动自身免疫紊乱,阻断型抗体可有效抑制异常免疫应答,是自免治疗的核心研究方向。
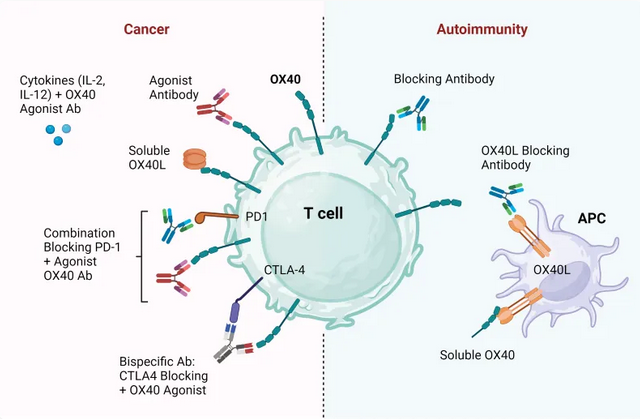
Figure 3. OX40在肿瘤和自免领域的转化
Rocatinlimab的全球临床终止,并非OX40靶点本身的生物学价值被否定,而是反向印证了行业共识:靶点临床转化的成功,始终建立在对其基础生物学机制的完整、深度认知之上,当前OX40领域的转化瓶颈,本质上正是底层基础研究的不足。本次事件直接暴露了领域内多个尚未破解的核心问题。
OX40信号在效应T细胞与Treg细胞中呈现完全不同的调控效应:激活效应T细胞表面的OX40可增强机体抗感染、抗肿瘤免疫,而调控Treg细胞表面的OX40则直接影响机体免疫稳态的维持。但领域内始终缺乏长期、系统性阻断OX40对免疫稳态影响的量化研究数据,无法明确长期阻断是否会削弱Treg介导的外周耐受与免疫监视、增加潜伏病毒再激活与肿瘤发生风险,Rocatinlimab临床试验中出现的卡波西肉瘤信号,正是这一认知空白的直接体现。
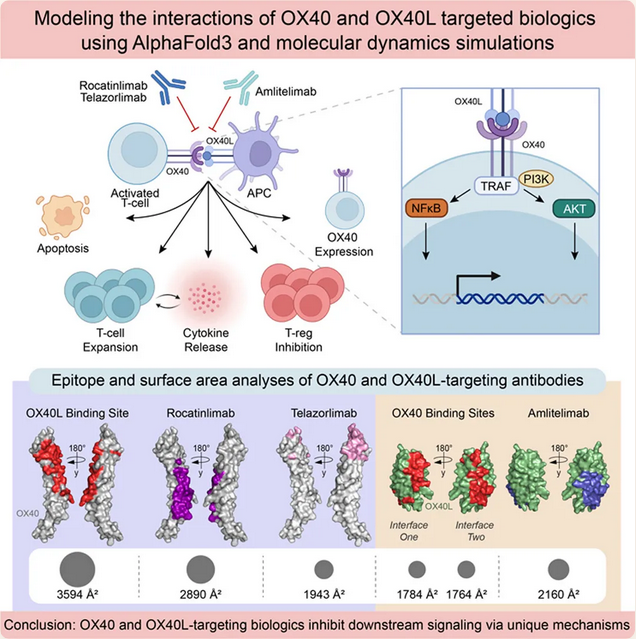
Figure 4. OX40信号在效应T细胞与Treg细胞中的调控
OX40的表达具有严格的时序性与组织微环境依赖性,其表达水平、阳性细胞亚群分布在不同疾病阶段、不同组织微环境、不同患者个体中存在极大异质性,不同细胞亚群中OX40干预后的功能结局也完全不同。自身免疫病治疗需要实现全身、长期的OX40通路阻断,但当前研究尚未完成对OX40在不同组织中细胞分布与功能差异的精准解析,无法实现对病灶与特定细胞亚群的精准靶向调控,最终导致“一刀切”式的全身阻断,引发不可控的免疫稳态偏移。
Rocatinlimab是一款具备ADCC效应的OX40阻断型抗体,其生物学活性受结合表位、亲和力、Fc段功能、交联活性等多个因素共同调控。但当前领域内对于OX40抗体分子设计与体内效应之间的构效关系,始终没有形成统一的认知:抗体结合表位、Fc段结合特性、亲和力高低如何影响阻断活性与体内安全性,目前仍无明确结论,导致OX40靶向抗体的分子设计缺乏明确的理论指导,无法精准预判抗体的体内效应与安全风险。
精准的患者分层是临床研究成功的核心前提,但当前OX40靶点的研发,仍缺乏经过大样本验证的预测性生物标志物。基础研究层面既未明确哪些自身免疫病患者的疾病进程由OX40通路过度活化真正驱动,也没有可用于筛查潜伏感染、免疫缺陷等用药风险因素的预警标志物,更无法建立用药后机体免疫功能的动态监测体系。生物标志物体系的缺失,直接导致临床研究无法实现精准的患者入组分层,既无法最大化药物的临床获益,也无法提前规避潜在的安全性风险。
Rocatinlimab的临床终止,为OX40领域的研发敲响了警钟,也推动整个行业重新回归靶点的基础科学研究。临床转化的瓶颈,恰恰是基础研究的核心机遇,未来OX40靶点的研究将重点围绕破解当前的核心认知空白展开:借助单细胞测序、空间转录组、质谱流式等技术,全面解析OX40在不同疾病、不同组织、不同细胞亚群中的表达特征与功能异质性;通过冷冻电镜等结构生物学研究,明确抗体-靶点结合的构效关系,建立OX40靶向分子理性设计的行业标准;深入阐释OX40在免疫监视与免疫稳态中的调控机制,量化靶点干预的剂量效应与安全边界;通过多组学技术系统挖掘疗效预测与风险预警的生物标志物,建立可用于临床的精准患者分层体系。
OX40作为机体免疫应答调控的核心共刺激分子,其生物学功能与转化价值已得到领域内的广泛认可。Rocatinlimab的全球临床终止,不是OX40靶点研究的终点,而是整个行业重新回归基础研究、完善底层生物学认知的新起点。只有深耕基础研究,完整破解靶点的核心科学问题,才能真正释放OX40靶点的转化应用潜力。
abinScience提供以下研究工具,适用于Western Blot、免疫组化、ELISA、流式细胞术及体内实验等多种研究场景,为OX40靶点的蛋白检测、细胞功能分析及动物水平验证提供系统支持。
| Product Name | Catalog No. |
| Recombinant Red fox CD134/TNFRSF4/OX40 Protein, C-His | ZW342012 |
| Recombinant Dog CD134/TNFRSF4/OX40 Protein, C-Fc | CW342012 |
| Recombinant Mouse CD134/TNFRSF4/OX40 Protein, N-His | MW342012 |
| Recombinant Human CD134/TNFRSF4/OX40 Protein, C-His | HW342011 |
| Recombinant Mouse CD134/TNFRSF4/OX40 Protein, C-Fc | MW342011 |
| Recombinant Human CD252/TNFSF4/OX40L Protein, C-His | HB937021 |
| Recombinant Human CD252/TNFSF4 Protein, N-His | HB937012 |
| Recombinant Human CD252/TNFSF4 Protein, N-Fc | HB937011 |
| Product Name | Catalog No. |
| Research Grade Anti-Human CD134/TNFRSF4/OX40 (INCAGN1949) | HW342086 |
| Research Grade Anti-Human CD134/TNFRSF4/OX40 (BAT6026) | HW342096 |
| Research Grade Anti-Human CD134/TNFRSF4/OX40 (BMS 986178) | HW342106 |
| Research Grade Anti-Human CD134/TNFRSF4/OX40 (INBRX-106) | HW342126 |
| Research Grade Rocatinlimab | HW342076 |
| Research Grade Gimistotug | HW342196 |
| Research Grade Ivuxolimab | HW342016 |
| Research Grade Pogalizumab | HW342026 |
| Anti-Human CD134/TNFRSF4/OX40 Antibody (SAA2011) | HW342013 |
| Anti-Human CD134/TNFRSF4/OX40 Antibody (3C8) | HW342307 |
| Anti-Human CD134/TNFRSF4/OX40 Monoclonal Antibody (1A641) | HW342035 |
| Anti-Mouse CD134/TNFRSF4/OX40 Antibody (OX-86) | MW342107 |
| InVivoMAb Anti-Mouse PD-L1 & OX40 Bispecific Antibody (Iv0244) | MW342010 |
| InVivoMAb Anti-Mouse CTLA4 & OX40 Bispecific Antibody | MB651040 |
查看更多OX40相关产品 →
[1] Fu Y, Lin Q, Zhang Z, Zhang L. Therapeutic strategies for the costimulatory molecule OX40 in T-cell-mediated immunity. Acta Pharm Sin B. 2020 Mar;10(3):414-433. doi: 10.1016/j.apsb.2019.08.010. Epub 2019 Sep 3. PMID: 32140389; PMCID: PMC7049610.
[2] Croft M. Control of immunity by the TNFR-related molecule OX40 (CD134). Annu Rev Immunol. 2010;28:57-78. doi: 10.1146/annurev-immunol-030409-101243. PMID: 20307208; PMCID: PMC2882161.
[3] Willoughby J, Griffiths J, Tews I, Cragg MS. OX40: Structure and function - What questions remain? Mol Immunol. 2017 Mar;83:13-22. doi: 10.1016/j.molimm.2017.01.006. Epub 2017 Jan 13. PMID: 28092803.
[4] Luo Y, Li J, Li L, Qin B, Zhou R, Tang Y. OX40 signaling in cancer immunotherapy: mechanisms of action, translational applications, and therapeutic perspectives. Front Immunol. 2026 Feb 9;17:1724756. doi: 10.3389/fimmu.2026.1724756. PMID: 41737211; PMCID: PMC12926375.
[5] Gupta AK, Steriopoulos J, Economopoulos V, Mirmirani P, Piguet V. OX40/OX40L modulation: A target for regulating T cells in cutaneous inflammatory disorders. J Eur Acad Dermatol Venereol. 2026 Apr 11. doi: 10.1111/jdv.70443. Epub ahead of print. PMID: 41964298.
[6] Nolden K, Shi Y, Batista VS, Bunick CG. Molecular differentiation of OX40- and OX40L-targeted biologics using AlphaFold3 and molecular dynamics simulations. J Invest Dermatol. 2026 Feb 4:S0022-202X(26)00073-4. doi: 10.1016/j.jid.2026.01.024. Epub ahead of print. PMID: 41651107; PMCID: PMC13047499.
本文所提供的所有产品与服务均仅供科研使用,不得用于人体诊断或治疗。
For Research Use Only. Not for use in diagnostic or therapeutic procedures.
返回顶部