
想象一下,早晨起床时还神采奕奕,午后却眼睑下垂、说话含糊,甚至连拿筷子的力气都没有。这就是重症肌无力患者的真实写照。重症肌无力(Myasthenia Gravis,简称MG)是一种自身免疫性神经肌肉疾病,主要特征是肌肉疲劳性和无力,影响神经肌肉接头(Neuromuscular Junction,NMJ)的信号传导。该病通常表现为波动性肌无力,症状可从眼肌开始(如眼睑下垂、复视),逐渐扩展到面部、咽喉、四肢和呼吸肌。
MG的发病率约为每年每百万人口中5-30例,多发于女性(尤其是20-40岁)和老年男性。约80-90%的患者血清中可检测到针对乙酰胆碱受体(AChR)的自身抗体,其他亚型包括针对肌肉特异性激酶(MuSK)或低密度脂蛋白受体相关蛋白4(LRP4)的抗体。MG可与胸腺瘤相关,胸腺异常在AChR阳性患者中常见。
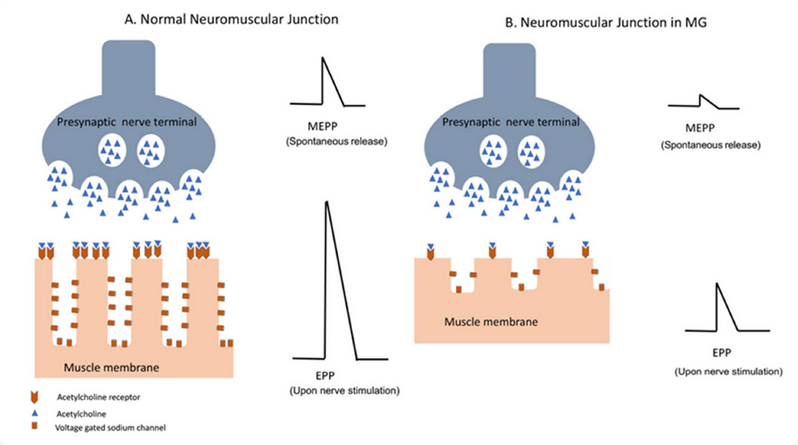
Figure 1. 正常个体(A)和肌萎缩侧索硬化症患者(B)的神经肌肉传递
临床上,MG可分为眼肌型(仅限眼部)和全身型(影响多组肌肉),严重时可导致呼吸衰竭(肌无力危象)。诊断依赖临床症状、血清抗体检测、重复电刺激测试和单纤维肌电图。预后一般良好,但需长期管理以控制症状。
MG的发病机制主要为自身免疫介导的NMJ功能障碍。核心是自身抗体针对NMJ后突触膜上的关键蛋白,导致乙酰胆碱(ACh)信号传导受阻。具体而言:
这些机制导致NMJ后突触膜破坏,安全因子降低,重复使用后肌无力加重。
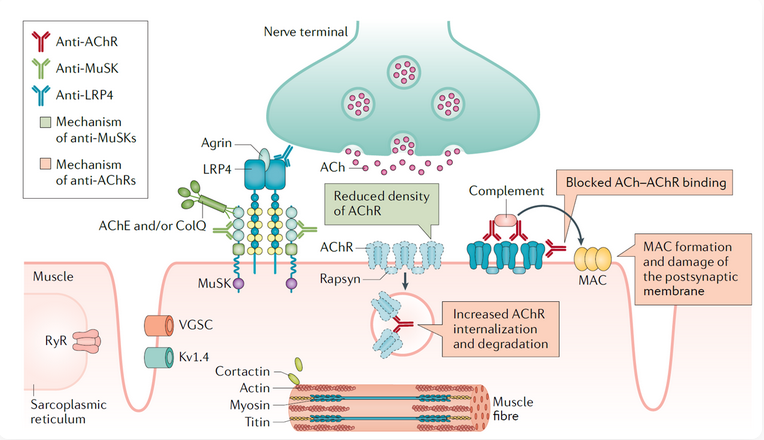
Figure 2. MG在神经肌肉接头的病理生理学
机制:AChR抗体(主要是IgG1/IgG3)激活经典补体途径,导致C5裂解形成膜攻击复合物(MAC),破坏突触后膜褶皱和AChR。C5抑制剂阻断C5裂解,防止MAC组装,避免NMJ破坏,而不影响上游补体功能。
代表药物(基于III期试验):
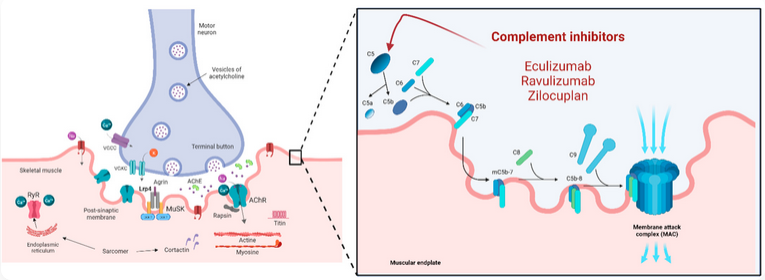
Figure 3. 补体抑制剂及其作用机制
机制:FcRn在酸性内体中结合IgG,防止其溶酶体降解并循环回收,导致致病IgG(包括AChR/MuSK抗体)半衰期延长。FcRn抑制剂竞争性阻断IgG-FcRn结合,加速IgG降解,快速降低循环IgG水平(通常降60–80%),从而减少NMJ损伤。
代表药物:
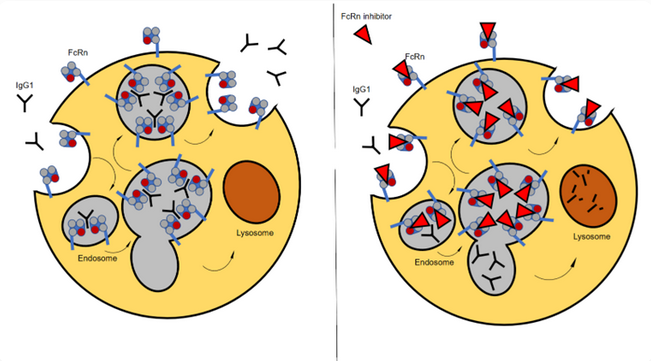
Figure 4. FcRn靶向作用机制
Rituximab (CD20单抗):耗竭CD20+ B细胞,MuSK+疗效最明确(常实现长期缓解),AChR+部分有效。
Inebilizumab (CD19单抗):2025晚期获批,长效(年2剂),针对更广B细胞谱。
CAR-T细胞疗法(针对致病浆细胞/B细胞):
这些新兴疗法代表从“非特异抑制”向“精准根除致病B/浆细胞”的转变,潜在实现长期无药缓解,但需关注感染风险、细胞因子风暴等。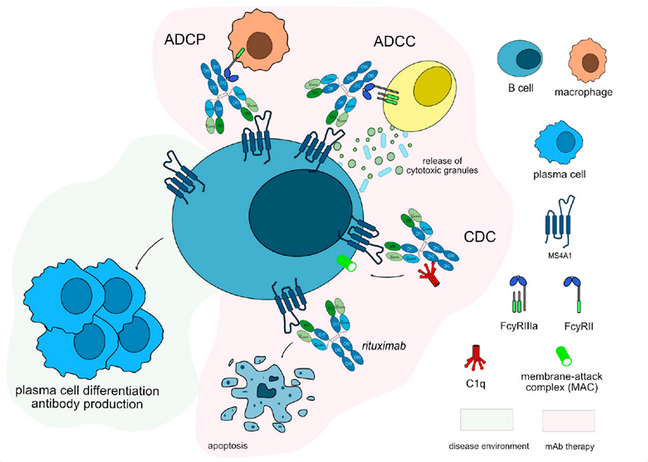
Figure 5. Rituximab的作用机制
以下为 abinScience 针对重症肌无力核心通路的重组蛋白与抗体产品,目录号可直接点击进入产品页。
| Catalog No. | Product name |
| HX061056 | Research Grade Efgartigimod |
| HB996026 | Research Grade Inebilizumab |
| HX061046 | Research Grade Nipocalimab |
| HF687016 | Research Grade Ravulizumab |
| HX061026 | Research Grade Rozanolixizumab |
| HF004126 | Research Grade Laprituximab |
| HY257056 | Research Grade Rituximab |
| HF687026 | Research Grade Eculizumab |
| AY257024 | Anti-Rituximab Polyclonal Antibody |
| AF687014 | Anti-Eculizumab Polyclonal Antibody |
| Catalog No. | Product name |
| HT005012 | Recombinant Human AGRN Protein, N-His |
| HF599012 | Recombinant Human LRP4 Protein, N-GST |
| HF687012 | Recombinant Human C5 Protein, N-GST |
| HF687022 | Recombinant Human C5 Protein, N-His |
| HF974012 | Recombinant Human HLA-DRB1 Protein, N-His |
| HF829012 | Recombinant Human CHRNA1 Protein, N-GST |
| HY041012 | Recombinant Human HMGCR Protein, N-His |
| HY328012 | Recombinant Human IL6 Protein, N-His |
| HY328011 | Recombinant Human IL6 Protein, C-His-Avi |
| HY328021 | Recombinant Human IL6 Protein, C-His |
| HY257012 | Recombinant Human CD20/MS4A1 Protein, N-His |
| HY257022 | Recombinant Human CD20/MS4A1 Protein, N-His-Trx |
| HY257011 | Recombinant Human CD20/MS4A1 Protein, N-His |
| HB990012 | Recombinant Human CD119/IFNGR1 Protein, N-His |
| HB990011 | Recombinant Human CD119/IFNGR1 Protein, C-His |
| HB651012 | Recombinant Human CD152/CTLA4 Protein, N-His |
| HB651011 | Recombinant Human CD152/CTLA4 Protein, C-His |
| HB199012 | Recombinant Human CD154/CD40LG/TNFSF5 Protein, C-His |
| HX061012 | Recombinant Human FCGRT Protein, N-His |
| HV212012 | Recombinant Human CD257/TNFSF13B Protein, N-His |
| HV212011 | Recombinant Human CD257/BAFF/TNFSF13B Protein, N-Fc |
| HV212021 | Recombinant Human CD257/BAFF/TNFSF13B Protein, C-His |
| HB199011 | Recombinant Human CD154/CD40LG/TNFSF5 Protein, C-His |
| HP394012 | Recombinant Human ZC3HAV1 Protein, N-His |
| HF829022 | Recombinant Human CHRNA1 Protein, N-His |
| HY328031 | Recombinant Human IL6 Protein, C-Fc |
| HF829032 | Recombinant Human CHRNA1 Protein, C-His |
| HC556012 | Recombinant Human TNIP1 Protein, N-His |
| HC556011 | Recombinant Human TNIP1 Protein, N-His |
| HT224012 | Recombinant Human MUSK Protein, N-His |
| HY328521 | Biotin-labeled Recombinant Human IL6 Protein, C-His |
| HB990021 | Recombinant Human CD119/IFNGR1 Protein, C-Fc |
| Catalog No. | Product name |
| AF687028 | Anti-Eculizumab Neutralizing Antibody ELISA kit |
| AF687018 | Anti-Eculizumab ELISA Kit |
| DF687028 | Eculizumab ELISA Kit |
| AY257018 | Anti-Rituximab ELISA Kit |
需要重症肌无力研究工具?
abinScience提供针对AChR、MuSK、LRP4、C5、FcRn等MG核心通路的高纯度重组蛋白、抗体及ELISA试剂盒,支持机制研究与药物开发。
技术咨询立即询价
联系邮箱:info@abinscience.com | 电话:027--87433958Reference:
返回顶部