
戊型肝炎病毒(HEV)是全球范围内急性病毒性肝炎的重要病原之一。HEV在传播方式和疾病谱上呈现出更加复杂的流行特征:一方面,HEV-1和HEV-2主要通过粪--口传播,在发展中国家流行;另一方面,HEV-3和HEV-4则具有明显的人畜共患特征,主要通过污染的肉制品传播,是发达国家急性戊肝的主要病因。
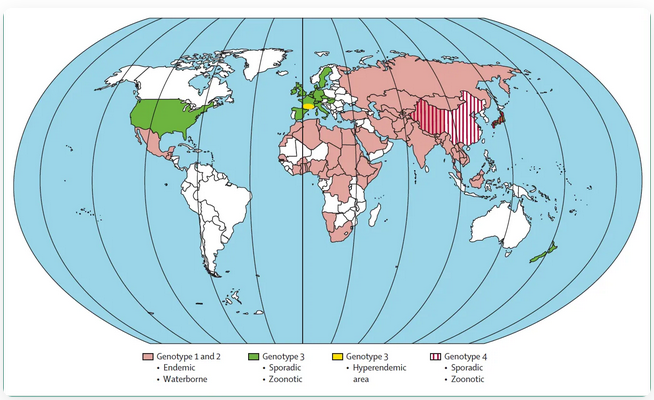
图1. HEV全球感染病例的分布情况
在多数免疫功能正常的个体中,HEV感染通常表现为自限性过程。然而,在免疫抑制人群(如器官移植受者)中,HEV-3和HEV-4可发展为慢性感染,进而导致肝纤维化甚至肝硬化。这一人群中的治疗问题,使HEV从“自限性病毒”转变为一个具有明确临床干预需求的研究对象。
长期以来,HEV的基础机制研究、抗病毒药物研发进展缓慢,慢性戊肝感染始终缺乏获批的特异性靶向治疗药物。近日,国际胃肠病学期刊《Gut》在线发表了北京大学、海德堡大学、波鸿鲁尔大学联合团队的重磅研究成果,该研究从模型系统构建与药物筛选策略两个层面同时推进,为HEV研究提供了新的技术路径,也带来了潜在的治疗突破。
本研究中值得关注的一点是其建立的全长HEV荧光报告系统。传统HEV药物筛选主要依赖亚基因复制子(subgenomic replicon),这类系统通常删除了ORF2和ORF3结构蛋白区域,虽然操作简便,但存在一个关键问题——无法完整反映病毒生命周期,尤其是:
? 缺失病毒装配与释放过程
? 忽略结构蛋白参与宿主免疫调控
? 对某些靶向结构蛋白的药物筛选能力不足
本研究在ORF2衣壳蛋白C端引入split GFP标签,构建了一个可以覆盖完整复制周期的报告系统。这一改进带来的意义在于:
? 将“复制”与“病毒结构功能”整合到同一筛选体系
? 可以同步评估抗病毒活性与细胞毒性(通过荧光与核染信号)
? 为后续靶向ORF2/ORF3的药物开发提供了直接实验基础
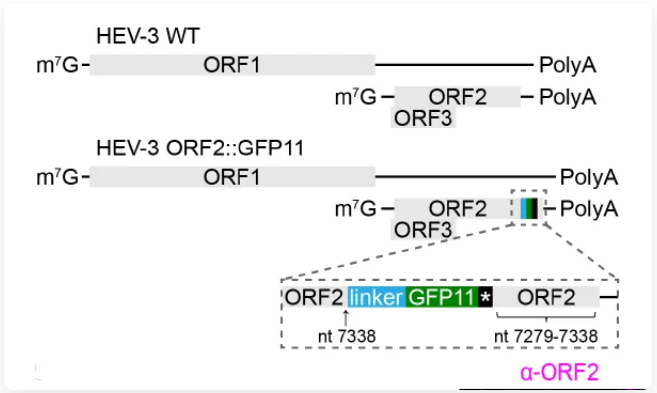
图2. 基于ORF2的全长HEV荧光报告系统
换句话说,这项工作实际上把HEV药物筛选,从“片段模型”推进到了“接近真实感染状态的系统级模型”。
基于该体系,研究对核苷(酸)类似物库进行了筛选,最终确定Bemnifosbuvir(BEM)为最具潜力的候选分子之一。从实验结果来看,这一分子的特点并不只是“有效”,而是具备几个对抗病毒研究尤为关键的属性:
1. 抑制作用明确且稳定
? 在体外细胞模型中表现出剂量依赖性抑制
? IC50约为0.54 μM,优于部分已报道候选分子
2. 跨模型一致性
不仅在常规肝癌细胞系中有效,在以下系统中同样成立:
? iPSC来源肝样细胞
? 原代人肝细胞(PHHs)
? 动物感染模型(沙鼠)
这说明其抗病毒作用具有一定的生理相关性。
3. 抗耐药潜力
长期传代(>160天)后病毒仍保持对BEM敏感,提示其可能具有较高的耐药屏障,这一点在RNA病毒研究中尤为关键。
4. 联合用药策略可行
与RBV联用呈现加和效应(部分条件下协同),为未来治疗方案提供现实路径,而不是完全替代现有体系。
该研究的价值不仅在于筛选出可快速推进临床的抗HEV候选药物,更在于为领域提供了标准化的新型研究模型,重新定义了ORF2衣壳蛋白在HEV研究中的核心地位,也催生了多个前沿研究方向。
1. ORF2功能机制的深度研究
该研究与近年多项成果共同证实,ORF2的生物学功能远超出传统认知的“结构蛋白”范畴,其在病毒免疫逃逸、跨物种传播、毒力调控、慢性感染维持等过程中均发挥关键作用。目前,不同基因型HEV ORF2的序列-功能差异、不同宿主来源(人、猪、禽类)HEV ORF2的跨物种感染机制、ORF2与宿主蛋白的互作网络、ORF2在病毒耐药中的调控作用等方向,均是领域内的研究热点。
2. 新型HEV研究模型的构建与验证
该研究构建的全长报告病毒为后续研究提供了范式。未来,不同基因型、不同宿主来源、不同突变株的全长报告病毒及感染性克隆的构建,均需要ORF2抗体作为核心工具,用于病毒感染效率定量、ORF2表达定位检测、病毒株鉴定等环节;同时需要重组ORF2蛋白作为实验体系的阳性对照。
3. 下一代抗HEV药物的研发
除靶向RdRp的核苷类似物外,靶向ORF2衣壳组装的抑制剂是下一代抗HEV药物的核心研发方向。这类药物的筛选与评价,需要重组ORF2蛋白开展体外衣壳组装实验、化合物结合实验,同时需要ORF2抗体评价化合物对病毒感染及ORF2功能的影响。
4. 人畜共患HEV的防控研究
HEV是典型的人兽共患病原体。除猪源HEV 3/4型外,禽类戊肝病毒(aHEV)不仅给家禽养殖业造成经济损失,还存在跨物种传播的潜在风险,是One Health理念下的重要研究方向。相关研究均需要对应的禽类HEV ORF2重组衣壳蛋白与特异性抗体作为核心支撑。
本研究是HEV领域技术研发与药物探索的一次重要突破。研究团队以ORF2衣壳蛋白为核心,成功构建的全长HEV荧光报告病毒与成像型高通量筛选平台,为HEV基础机制探索、抗病毒药物高通量筛选建立了更贴合实际的技术体系,也为后续相关研究的开展提供了可借鉴的标准化实验范式。
为助力广大科研工作者开展HEV研究、抗病毒药物研发、人畜共患病防控、疫苗开发等相关工作,abinScience可提供多种HEV相关抗体与蛋白,产品聚焦ORF2靶点,覆盖人源、禽类等多物种。
| Product Name | Catalog No. |
| InVivoMAb Anti-Hepatitis E virus/HEV pORF2 P domain Neutralizing Antibody (Iv0278) | VK620020 |
| Anti-Hepatitis E virus/HEV pORF2 P domain Neutralizing Antibody (SAA2238) | VK620023 |
| Anti-Hepatitis E virus/HEV pORF2 P domain Neutralizing Antibody (SAA2239) | VK620033 |
| Anti-Hepatitis E virus/HEV pORF2 P domain Neutralizing Antibody (SAA2240) | VK620043 |
| Anti-HEV Capsid protein Antibody (8G12) | VK620013 |
| Anti-Avian HEV Capsid Polyclonal Antibody | VK620034 |
| Anti-Hepatitis E virus genotype 1/HEV-1 ORF2 Polyclonal Antibody | VK620014 |
| Anti-Hepatitis E virus genotype 1/HEV-1 ORF2 Polyclonal Antibody | VK620024 |
| Recombinant Avian HEV Capsid Protein, N-His | VK620032 |
更多HEV相关研究产品欢迎咨询或发邮件给我们: support@abinscience.com
[1]
Kamar N, Bendall R, Legrand-Abravanel F, Xia NS, Ijaz S, Izopet J,
Dalton HR. Hepatitis E. Lancet. 2012 Jun 30;379(9835):2477-2488. doi:
10.1016/S0140-6736(11)61849-7. Epub 2012 Apr 30. Erratum in: Lancet.
2012 Aug 25;380(9843):730. PMID: 22549046.
[2]
Letafati A, Taghiabadi Z, Roushanzamir M, Memarpour B, Seyedi S,
Farahani AV, Norouzi M, Karamian S, Zebardast A, Mehrabinia M, Ardekani
OS, Fallah T, Khazry F, Daneshvar SF, Norouzi M. From discovery to
treatment: tracing the path of hepatitis E virus. Virol J. 2024 Aug
23;21(1):194. doi: 10.1186/s12985-024-02470-3. Erratum in: Virol J. 2024
Sep 10;21(1):214. doi: 10.1186/s12985-024-02490-z. PMID: 39180020;
PMCID: PMC11342613.
[3]
Debing Y, Moradpour D, Neyts J, Gouttenoire J. Update on hepatitis E
virology: Implications for clinical practice. J Hepatol. 2016
Jul;65(1):200-212. doi: 10.1016/j.jhep.2016.02.045. Epub 2016 Mar 8.
PMID: 26966047.
[4]
Guu TS, Liu Z, Ye Q, Mata DA, Li K, Yin C, Zhang J, Tao YJ. Structure
of the hepatitis E virus-like particle suggests mechanisms for virus
assembly and receptor binding. Proc Natl Acad Sci U S A. 2009 Aug
4;106(31):12992-7. doi: 10.1073/pnas.0904848106. Epub 2009 Jul 21. PMID:
19622744; PMCID: PMC2722310.
[5]
Hu J, Liu T, Kl?hn M, Freistaedter A, Toprak E, Chi H, G?mer A,
Pottkaemper L, Jordan P, Yang X, Zhang H, Becker J, Nkongolo S, Lohmann
V, Steinmann E, Wang L, Dao Thi VL. Nucleotide analogue bemnifosbuvir
inhibits hepatitis E virus replication in preclinical models. Gut. 2026
Mar 6:gutjnl-2025-336714. doi: 10.1136/gutjnl-2025-336714. Epub ahead of
print. PMID: 41791851.
返回顶部