
亨廷顿病(Huntington's disease, HD)最早于1872年由美国医师George Huntington系统描述,因此以其姓氏命名。该病是一种完全外显的常染色体显性遗传病,患者只要继承一个突变等位基因即可发病,具有典型的“遗传早现”现象——子代发病年龄往往早于亲代。全球患病率约为10万人中5–10例,中国人群略低但近年诊断率显著上升。典型症状包括无法控制的舞蹈样运动(chorea)、精神障碍以及进行性认知功能减退,通常在中年内(30–50岁)起病,病程10–25年,最终因吞咽困难、肺炎或心衰离世。
HD 的根本致病机制是 HTT 基因(编码 Huntingtin 蛋白) 第1外显子中 CAG 三核苷酸重复序列异常扩增。扩增的 CAG 编码异常延长的聚谷氨酰胺(polyQ)链,使 Huntingtin 蛋白获得毒性功能(toxic gain-of-function):诱导蛋白错误折叠与聚集、干扰转录调控、破坏轴突运输、抑制自噬清除、阻断 BDNF 产生与运输,并最终导致纹状体中等棘突神经元(MSNs)和皮质神经元选择性死亡。
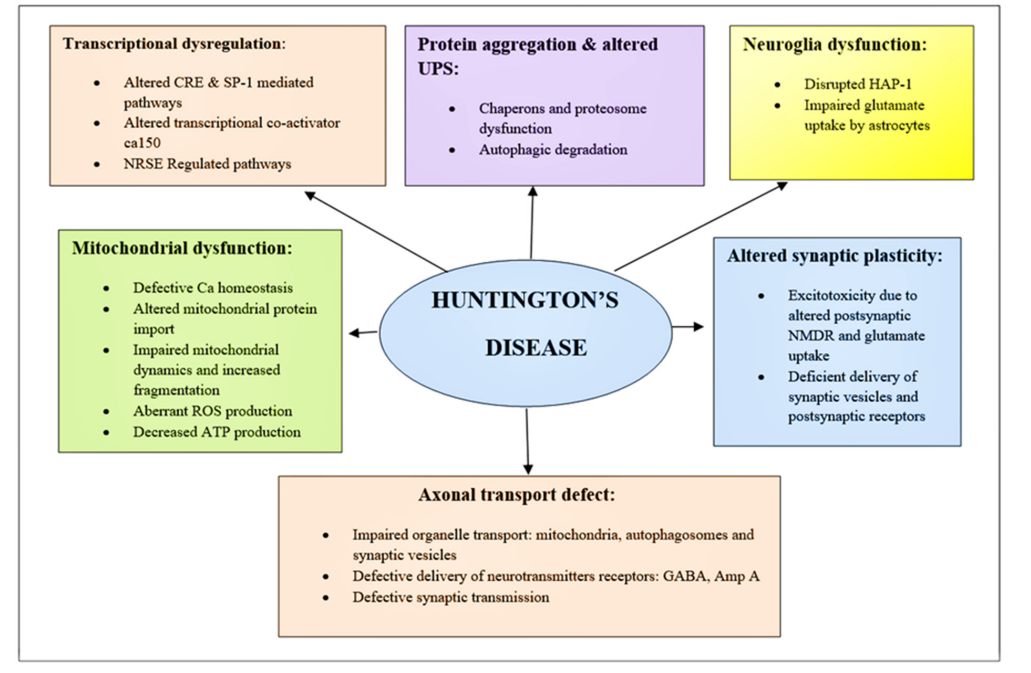
Fig 1.Schematic of diverging pathways leading to the pathogenesis of HD(doi.org/10.3390/brainsci12101389)
HD 虽由单一基因突变驱动,但其下游病理网络高度复杂,涉及蛋白质稳态失调、神经营养缺失、自噬障碍、兴奋毒性、线粒体功能异常等多条通路。以下表格系统梳理了当前公认的核心靶点及其在 HD 中的作用机制,为靶向干预提供理论基础。
| 靶点 | 正常生物学功能 | HD 中的病理角色 | 研究应用 |
| HTT (Huntingtin) | 支架蛋白,参与囊泡运输、BDNF 支持、自噬和纤毛功能 | polyQ 扩展 → 毒性获得、蛋白聚集、转录失调、轴突运输障碍 | mHTT 聚集 ELISA、清除实验、HTT-lowering 验证 |
| BDNF / TrkB | 神经营养因子及其受体,维持纹状体神经元存活与突触可塑性 | 突变 HTT 抑制 BDNF 转录与轴突运输,导致神经营养缺失 | BDNF ELISA、TrkB 磷酸化检测、神经营养保护实验 |
| mTOR | 调控自噬、蛋白合成与细胞生长 | 异常激活抑制自噬,加剧 mHTT 积累与神经元损伤 | 自噬流检测、mTOR 抑制剂筛选 |
| GRIN2B (NMDAR) | NMDA 受体亚基,参与突触传递与可塑性 | 突触外过度激活引发兴奋毒性与钙超载 | 钙成像、兴奋毒性模型、NMDAR 拮抗剂筛选 |
治疗学意义:直接降低 HTT(ASO、RNAi、基因编辑)、激活 BDNF-TrkB 通路、调控 mTOR 促进自噬、以及选择性阻断突触外 NMDAR 是当前最具前景的疾病修正策略。
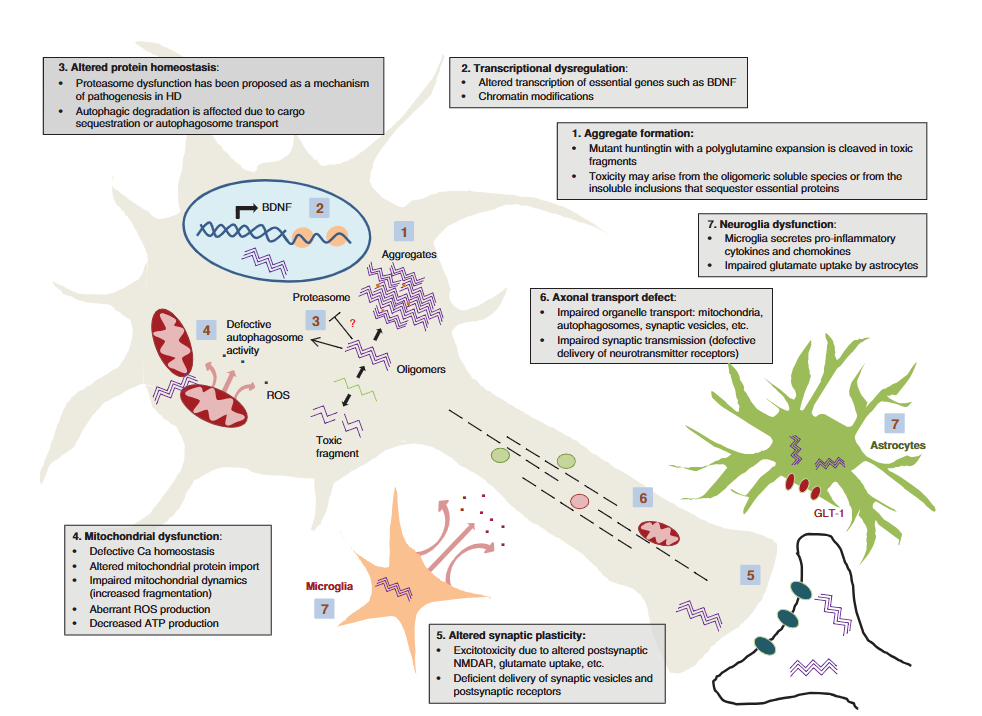
Fig 2. Schematic of selected mechanisms of pathogenesis in Huntington’s disease (HD)( 10.1101/cshperspect.a024240)
下表汇总来自期刊、临床试验注册库及权威机构的 HD 关键临床与基础研究突破。
| 主题 | 关键发现/试验结果 | 发布/更新时间 | 潜在影响 | 引用 |
| AMT-130(uniQure AAV-miHTT) | Phase I/II 36个月中期分析:高剂量组显示疾病进展趋势性减缓(cUHDRS改善75%,P=0.003)、CSF NfL低于基线,安全性可控 | 2024年10月 | 显示潜在疾病修正效果的HD基因治疗,有望成为one-time疗法里程碑 | [1] |
| Tominersen(Roche) | GENERATION HD2中期分析后调整为仅保留100mg剂量组继续进行;此前高剂量方案因风险/获益问题终止 | 2025更新 | 探索更年轻、低疾病负担患者中非等位基因选择性HTT-lowering的可行性 | [2] |
| WVE-003(Wave Life Sciences) | 等位基因特异性ASO;SELECT-HD早期数据显示~40–50% mHTT降低,同时保留野生型HTT,与尾状核萎缩减缓相关 | 2025数据 | 等位基因特异性方法的临床验证,为更大患者群体提供精准治疗范式 | [3] |
亨廷顿病(HD)目前的研究难点
多篇综述指出,HD 的最大障碍不是缺乏治疗方案,而是缺乏能够在早期准确反映病程变化的生物标志物,使 HTT-lowering 等干预难以被快速验证(Tong et al., IJMS, 2024)。同时,mHTT 聚集、BDNF-TrkB 缺失、自噬障碍与兴奋毒性共同驱动神经元损伤,正如 Piao et al.(Protein & Cell, 2025)所强调的,单一靶点干预很难改变疾病轨迹。越来越多研究因此转向多通路系统性调控,为 HD 治疗寻找更稳固的突破口。这些难点也凸显了多通路、多靶点系统研究的重要性——abinScience提供的BDNF-TrkB、mTOR、NMDAR相关工具正是为此而生。
以下为 abinScience 针对亨廷顿病核心通路的重组蛋白与抗体新产品,目录号可直接点击进入产品页。
为什么选择 abinScience 的 HD 研究工具?| Type | Catalog # | Product Name |
| Protein | MB935012 | Recombinant BDNF Protein, N-His |
| HB935012 | Recombinant Human BDNF Protein, N-His | |
| HB935022 | Recombinant Human BDNF Protein, N-His | |
| HC330012 | Recombinant Human GRIN2B Protein, N-His | |
| HW733012 | Recombinant Human MTOR Protein, N-His | |
| HW733022 | Recombinant Human MTOR Protein, N-His | |
| HS892012 | Recombinant Human TrkB /NTRK2 Protein, N-His | |
| Antibody | HS892016 | Research Grade Anti-Human TrkB /NTRK2 (ZEB85) |
| HB935014 | Anti-BDNF Polyclonal Antibody | |
| HC330014 | Anti-GRIN2B Polyclonal Antibody | |
| HB935107 | Anti-Human BDNF Antibody (SAA0471) | |
| HB935137 | Anti-Human BDNF Antibody (SAA0471), APC | |
| HB935117 | Anti-Human BDNF Antibody (SAA0471), FITC | |
| HB935127 | Anti-Human BDNF Antibody (SAA0471), PE | |
| HB935147 | Anti-Human BDNF Antibody (SAA0471), PerCP | |
| HW733013 | Anti-Human MTOR Antibody (SAA2296) | |
| HW733014 | Anti-Human MTOR Polyclonal Antibody | |
| HS892107 | Anti-Human TrkB /NTRK2 Antibody (SAA0477) | |
| HS892137 | Anti-Human TrkB /NTRK2 Antibody (SAA0477), APC | |
| HS892117 | Anti-Human TrkB /NTRK2 Antibody (SAA0477), FITC | |
| HS892127 | Anti-Human TrkB /NTRK2 Antibody (SAA0477), PE | |
| HS892147 | Anti-Human TrkB /NTRK2 Antibody (SAA0477), PerCP | |
| HS892014 | Anti-TrkB /NTRK2 Polyclonal Antibody | |
| HB935010 | InVivoMAb Anti-Human BDNF (Iv0093) |
Contact our scientific support team: support@abinscience.com
TEL: +86-027-65523339
abinScience:用高品质重组蛋白与精准抗体赋能亨廷顿病研究,并在帕金森病、阿尔茨海默病、亨廷顿病、多发性硬化等神经退行性疾病领域搭建关键靶点重组蛋白与抗体矩阵。
返回顶部