
银屑病是一类由遗传、环境与免疫因素共同驱动的免疫介导性慢性炎症性皮肤病,无传染性但病程迁延反复,严重影响患者生活质量,也是全球范围内亟待攻克的重要科研课题。从全球流行现状来看,其患病率存在显著地域与种族差异,总体介于0.1%~8%之间,其中白种人群患病率相对较高,可达2%~5%,全球累计受累人群已超1.25亿。
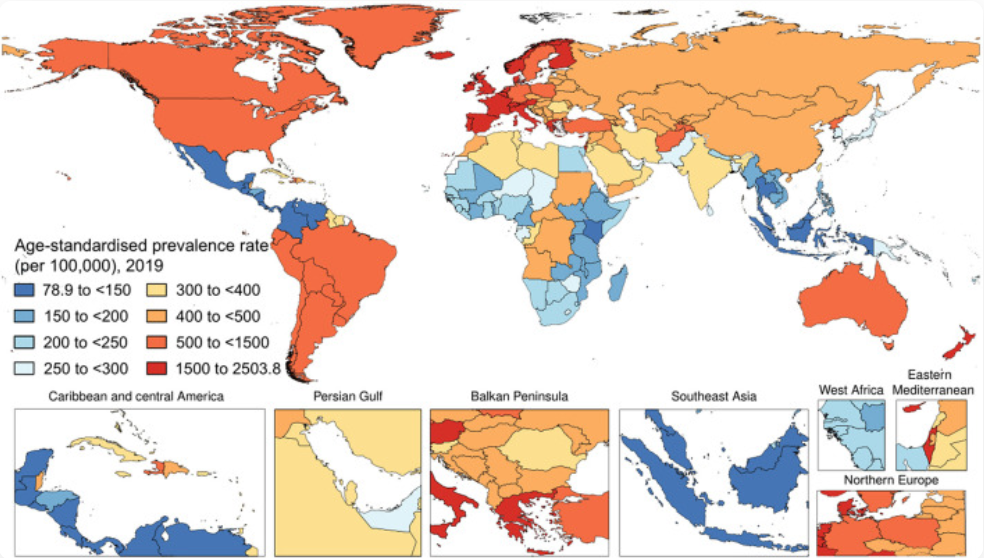
图1. The national age-standardized prevalence rate of psoriasis (per 100,000) in 2019
银屑病的核心发病机制表现为免疫紊乱驱动的炎症信号通路异常激活,最终形成“免疫细胞-细胞因子-角质形成细胞”的恶性循环。具体而言,环境诱因可激活真皮层树突状细胞等抗原提呈细胞,使其释放TNF-α、IL-12、IL-23等一系列促炎因子;这些因子进一步诱导CD4+ T细胞向Th17细胞定向分化并大量增殖,而Th17细胞会分泌IL-17A、IL-17F、IL-22等关键效应因子。其中,IL-17A是驱动皮损形成的核心分子,可直接作用于角质形成细胞,导致其异常增殖、分化障碍,同时释放更多炎症介质与趋化因子,招募中性粒细胞等炎症细胞浸润皮损部位。此外,IL-17A还能通过激活STAT3信号通路促进角蛋白K17表达,进一步加剧局部炎症反应;而成纤维细胞、内皮细胞等非免疫细胞也会参与炎症微环境的构建,与免疫细胞相互作用形成持续的炎症放大循环,最终导致皮损区域的慢性炎症与组织重塑。
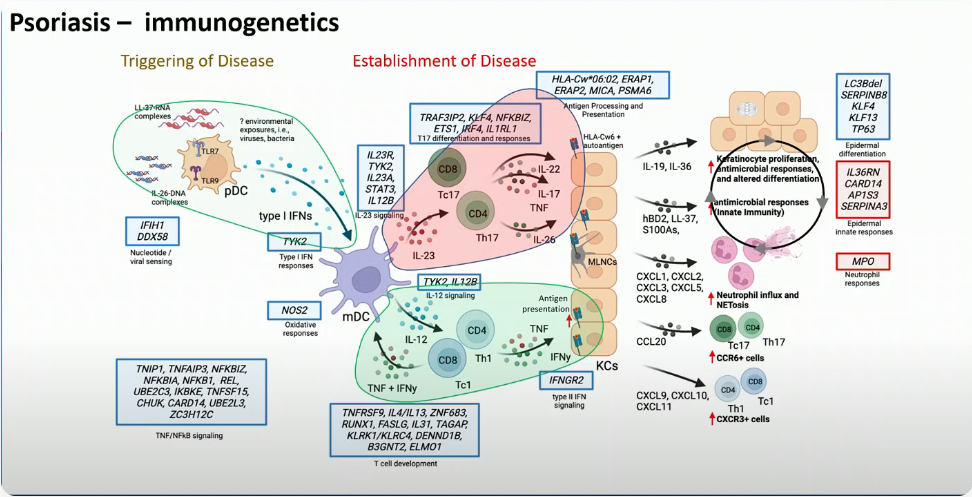
图2. 不同细胞因子介导银屑病
? TNF-α:作为促炎因子的上游枢纽,TNF-α放大炎症信号,促进免疫反应。阿达木单抗、英夫利昔单抗等单抗药物已被广泛应用于临床治疗。
? IL-17:IL-17是驱动皮损形成的重要效应因子,相关的抗IL-17单抗(如司库奇尤单抗、依奇珠单抗)及IL-17A/F双靶点单抗已成为中重度银屑病治疗的关键药物。
? IL-12/IL-23:IL-12与IL-23通过共享p40亚基调控Th1/Th17细胞的分化,靶向IL-12/IL-23的单抗(如乌司奴单抗、古塞奇尤单抗)能够从源头抑制免疫紊乱。
? IL-22/IL-36:IL-22与IL-17协同作用,促进角质形成细胞的异常增殖并维持皮损慢性炎症,相关单抗仍在临床研发阶段;IL-36则在泛发性脓疱型银屑病中发挥核心作用,靶向IL-36受体的佩索利单抗已获临床批准。
? JAK:JAK能够介导多个促炎因子的下游信号,相关小分子抑制剂如托法替布已获得临床批准,并且研发者正在继续推进高选择性JAK亚型抑制剂的研究,以提高治疗的安全性。
? JAK2:JAK2在免疫反应中发挥着重要作用,抑制JAK2的药物如芦可替尼,在炎症调控中的研究显示出较大潜力。
? JAK3:JAK3是关键的免疫细胞激活因子,开发高选择性JAK3抑制剂,能够精准地阻断免疫细胞的活化,从而在免疫疾病的治疗中展现出前景。
? TYK2:主要介导IL-12和IL-23的信号传导,TYK2的高选择性变构抑制剂已获得上市,具备精准抗炎和口服方便的优势。
? STAT3:STAT3是IL-17等促炎因子的下游核心转录因子,直接调控炎症基因表达及角质形成细胞的异常增殖。当前的研究主要集中于开发特异性STAT3抑制剂,以阻断炎症反应的终端放大过程,相关小分子药物目前处于临床前研发阶段。
? HIF1α:HIF1α作为IL-17A的下游靶分子,通过调控代谢重编程来增强炎症环路,其特异性抑制剂在体外实验中已显示出抗炎效果,并具有潜在的临床应用价值。
? PDE4:PDE4通过降解cAMP,增强炎症细胞的活性,促进炎症反应。阿普米司特等PDE4抑制剂能够提高cAMP水平,广谱抑制促炎因子的分泌,已成为中轻度银屑病的常用治疗药物。
? PDE7:PDE7具有与PDE4类似的功能,研究表明,PDE7抑制剂可以与PDE4抑制剂联合使用,增强抗炎效果并减少毒性,目前仍在临床前研究阶段。
? IRAK4:IRAK4位于IL-1R/TLR通路的核心,兼具激酶与支架功能,能够整合多条炎症信号通路。科研重点正在开发能够同时抑制其双重功能的抑制剂,目前相关药物仍处于临床前研究阶段。
? TAK1:TAK1能够整合IL-1、TNF-α等多条信号通路,其抑制剂在动物模型中展现出减轻皮损炎症的效果,临床转化研究正在推进。
以下为 abinScience 针对银屑病新产品,目录号可直接点击进入产品页。
| 作用靶点 | 目录号(Catalog No.) | 产品名称(Product name) |
| IL-17A | HS856026 | Research Grade Secukinumab |
| IL-17RA | HV263016 | Research Grade Brodalumab |
| IL-17A IL-17F | HS856036 | Research Grade Bimekizumab |
| IL-23p19 | HV466036 | Research Grade Guselkumab |
| TNF-α | HF879296 | Research Grade Etanercept |
| IL-12/IL-23 | HB769016 | Research Grade Ustekinumab |
| IL-4/IL-13 | HB732016 | Research Grade Dupilumab |
| 目录号(Catalog No.) | 产品名称(Product name) |
| AV466013 | Anti-Guselkumab Non-Neutralizing Antibody |
| AF879013 | Anti-Etanercept Non-Neutralizing Antibody |
| HF879010 | InVivoMAb Anti-Human TNFa/TNF-alpha (Iv0050) |
| HS856010 | InVivoMAb Anti-Human IL17A (Iv0029) |
| HB829014 | Anti-JAK1 Polyclonal Antibody |
| HC515014 | Anti-Human PDE4C Polyclonal Antibody |
| HT250014 | Anti-Human TRAF3IP2 Polyclonal Antibody |
| HV466010 | InVivoMAb Anti-Human IL23A (Iv0034) |
| HV466013 | Anti-Human IL23A/IL-23p19 Nanobody (SAA1160) |
| 目录号(Catalog No.) | 产品名称(Product name) |
| DS856028 | Bimekizumab ELISA Kit |
| DS856058 | Secukinumab ELISA Kit |
| AS856518 | Anti-Secukinumab Neutralizing Antibody ELISA kit |
| DV466028 | Guselkumab ELISA Kit |
| AV466028 | Anti-Guselkumab ELISA Kit |
| DV466018 | Mirikizumab ELISA Kit |
| AV466018 | Anti-Mirikizumab ELISA Kit |
| DF879058 | Etanercept ELISA Kit |
| AF879058 | Anti-Etanercept ELISA Kit |
| AF879518 | Anti-Etanercept Neutralizing Antibody ELISA kit |
abinScience提供经过严格验证的高质量银屑病研究工具,包括抗体、ELISA试剂盒和药物对照抗体,覆盖银屑病相关核心靶点,能帮您精准定位靶点、顺利推进实验研究。
[1] Damiani G, Bragazzi NL, Karimkhani Aksut C, Wu D, Alicandro G, McGonagle D, Guo C, Dellavalle R, Grada A, Wong P, La Vecchia C, Tam LS, Cooper KD, Naghavi M. The Global, Regional, and National Burden of Psoriasis: Results and Insights From the Global Burden of Disease 2019 Study. Front Med (Lausanne). 2021 Dec 16;8:743180. doi: 10.3389/fmed.2021.743180. PMID: 34977058; PMCID: PMC8716585.
[2] Li D, Fan S,
Song J, Zhao H, Guo L, Li P, Xu X. Global Psoriasis Burden 1990-2021:
Evolving Patterns and Socio-Demographic Correlates in the Global Burden
of Disease 2021 Update. Healthcare (Basel). 2025 Sep 26;13(19):2437.
doi: 10.3390/healthcare13192437. PMID: 41095525; PMCID: PMC12524270.
[3] Greb JE,
Goldminz AM, Elder JT, Lebwohl MG, Gladman DD, Wu JJ, Mehta NN, Finlay
AY, Gottlieb AB. Psoriasis. Nat Rev Dis Primers. 2016 Nov 24;2:16082.
doi: 10.1038/nrdp.2016.82. PMID: 27883001.
[4] Yang Y, Zhou
X, Wang W, Dai H. Glycobiology of psoriasis: A review. J Autoimmun. 2025
Feb;151:103361. doi: 10.1016/j.jaut.2025.103361. Epub 2025 Jan 13.
PMID: 39808852.
[5] Grayson M. Psoriasis. Nature. 2012 Dec 20;492(7429):S49. doi: 10.1038/492S49a. PMID: 23254969.
[6] Crow JM. Psoriasis uncovered. Nature. 2012 Dec 20;492(7429):S50-1. doi: 10.1038/492S50a. PMID: 23254970.
[7] Boehncke WH,
Sch?n MP. Psoriasis. Lancet. 2015 Sep 5;386(9997):983-94. doi:
10.1016/S0140-6736(14)61909-7. Epub 2015 May 27. PMID: 26025581.
[8] Griffiths CE,
Barker JN. Pathogenesis and clinical features of psoriasis. Lancet. 2007
Jul 21;370(9583):263-271. doi: 10.1016/S0140-6736(07)61128-3. PMID:
17658397.
[9] Ji C, Wang H,
Bao C, Zhang L, Ruan S, Zhang J, Gong T, Cheng B. Challenge of Nail
Psoriasis: An Update Review. Clin Rev Allergy Immunol. 2021
Dec;61(3):377-402. doi: 10.1007/s12016-021-08896-9. Epub 2021 Sep 3.
PMID: 34478047.
[10] Korman NJ.
Management of psoriasis as a systemic disease: what is the evidence? Br J
Dermatol. 2020 Apr;182(4):840-848. doi: 10.1111/bjd.18245. Epub 2019
Oct 15. PMID: 31225638; PMCID: PMC7187293.
返回顶部